Динамическое культивирование клеток
|
|
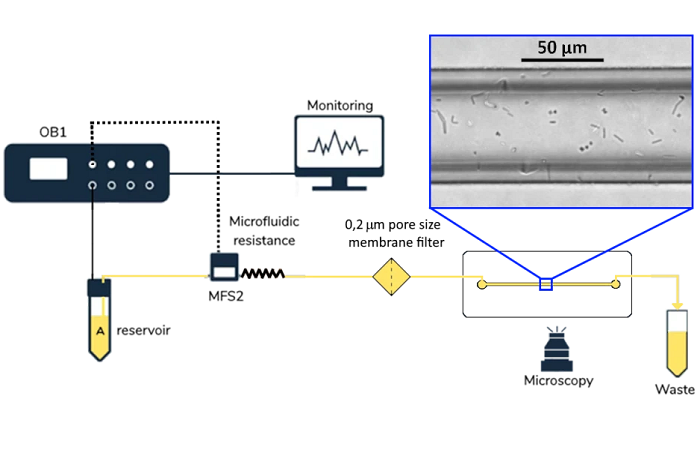
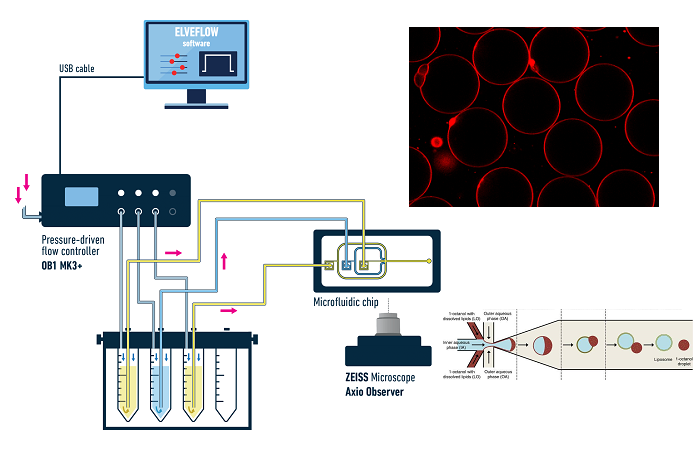
В организме человека на клетки и ткани действуют многочисленные силы, но они практически отсутствуют в традиционных установках для культивирования клеток, которые являются статичными. Микрофлюидные системы позволяют контролировать поток жидкости и механические нагрузки на клетки, выращиваемые in vitro. Динамичная культуральная среда способствует непрерывному переносу питательных веществ, метаболитов и отходов, а также добавляет напряжение сдвига. Это важный регулятор механочувствительных клеточных процессов, таких как пролиферация, выравнивание и ремоделирование. Подробнее о динамическом культивировании клеток Вы можете узнать из вебинара от эксперта Elveflow Лизы Муйжниекс. |
Вебинар Elveflow: Культивирование клеток в динамических условиях
Преимущества динамического культивирования
В этом руководстве описывается, как окрашивать клетки после динамического культивирования клеток. Окрашивание с помощью контроллера микрожидкостного потока OB1 Elveflow позволяет поддерживать точную скорость потока промывочного буфера и красителей над клетками в перфузионной камере. Автоматизация последовательности позволяет освободить время для многокрасочных анализов и повторных экспериментов. Подходит для термочувствительных красителей и небольших объемов. Читайте также наши заметки об автоматизации посева клеток и микрофлюидной перфузии для динамического культивирования клеток.
Некоторые основные области применения динамического культивирования клеток включают:
- Визуализация живых клеток (например, визуализация кальция, FISH);
- Скрининг лекарственных препаратов;
- Работа с напряжением сдвига;
- Анализ адгезии клеток: иммунный ответ, раковая инвазия и метастазирование;
- Модели физиологии и заболеваний: Органы на чипе, формирование и окклюзия кровеносных сосудов (атеросклероз), гомеостаз костной ткани и заболевания (остеопороз) и т.д.
Компоненты систем для автоматизированного посева клеток
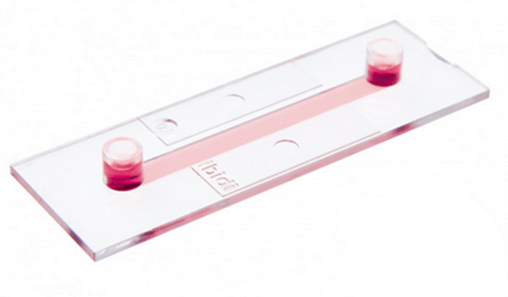
Характеристики слайд-камеры ibidi c 1 каналом
|
Параметры |
Значения |
|
Внешние размеры |
25.5 х 75.5 мм2 |
|
Длина канала |
50 мм |
|
Ширина канала |
5 мм |
|
Адаптер |
Female |
|
Объем резервуара |
60 µl |
|
Зона роста |
2.5 см2 |
|
Площадь покрытия |
5.2 / 5.4 / 5.6 / 5.8 см2 |
|
Дно: Защитное полимерное стекло ibidi | |
Комплектующие набора Elveflow
| Система распределения жидкости | ||
Схема установки для окрашивания клеток
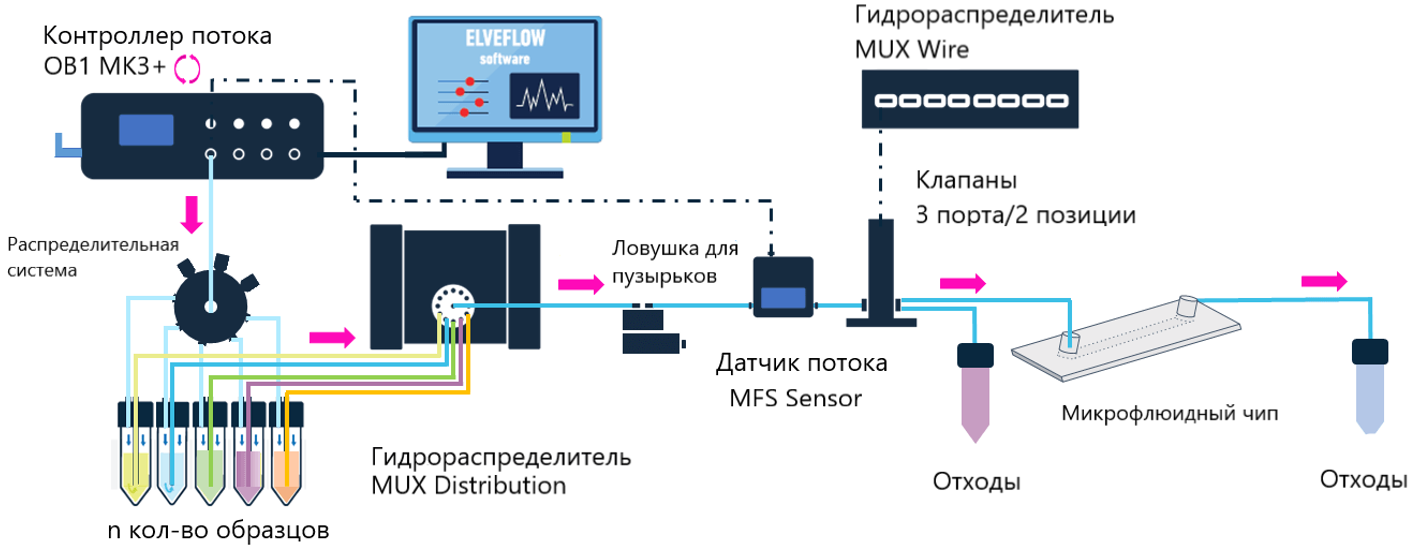
|
Оборудование
|
Реактивы
|
Если используемый микрофлюидный чип не обработан и/или не стерилен, вот два шага для подготовки культуральной камеры:
- Промойте микрофлюидный чип аниозимом (1%, 30 мин), тщательно ополосните водой и стерилизуйте в автоклаве или плазмотроне (в зависимости от материала чипа).
- Обработайте поверхность покрытием для адгезии клеток (например, коллагеном I или фибронектином).
Процесс автоматизированного окрашивания клеток в микрофлюидном канале
Краткое описание процесса
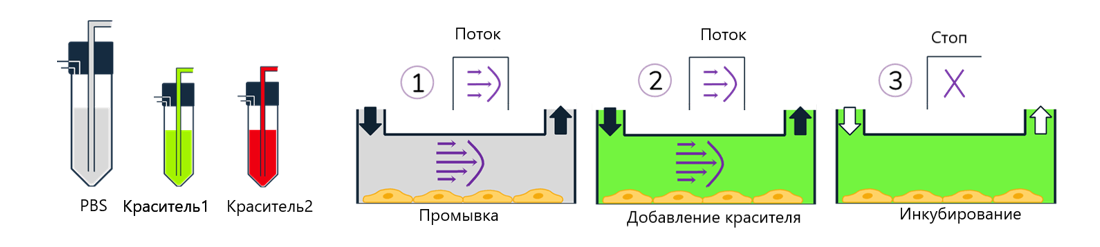
- Промывка: переключите вход MUX-Distributor на поток PBS, чтобы аккуратно промыть клетки.
- Добавьте краситель 1: переключите вход MUX-Distributor на поток красителя 1 и осторожно заполните канал красителями.
- Инкубация: остановите поток и удерживайте его, пока клетки впитывают краситель.
- Промыть: переключите вход MUX-Distributor на поток PBS, чтобы аккуратно смыть пятно 1.
- Дополнительные красители: Повторяйте шаги "Промывка", "Добавление красителя" и "Инкубация", пока клетки не будут окрашены.
- Промывка: переключите вход MUX-Distributor на проточный PBS, чтобы аккуратно промыть клетки.
Подробное руководство по окрашиванию клеток
Подключение приборов для автоматического окрашивания клеток
- Подключите контроллер OB1 к внешнему источнику давления с помощью пневматических трубок и к компьютеру с помощью USB-кабеля. Подробные инструкции по настройке контроллера давления OB1 можно найти в "Руководстве пользователя OB1".
- Подключите датчик потока к OB1, а клапан - к распределителю MUX.
- Подключите систему рециркуляции MUX и MUX Wire к компьютеру.
- Включите OB1, нажав на кнопку питания.
- Запустите программное обеспечение Elveflow. Основные функции и опции интеллектуального интерфейса Elveflow описаны в "Руководстве пользователя ESI". Пожалуйста, обратитесь к этому руководству за подробным описанием.
- Нажмите: добавить прибор \ выберите OB1 \ установите как MK3+, установите каналы давления, если необходимо, дайте имя прибору и нажмите OK для сохранения изменений. Теперь ваш OB1 должен появиться в списке распознанных устройств.
- Для первого использования требуется калибровка OB1. Пожалуйста, обратитесь к "Руководству пользователя OB1".
- Добавить датчик потока: нажмите: Добавить датчик \ выберите датчик скорости потока \ аналоговый или цифровой (выберите рабочий диапазон потока для датчика, если у вас аналоговый датчик), дайте имя датчику, выберите к какому устройству и каналу подключен датчик и нажмите OK для сохранения изменений. Ваш датчик потока должен появиться в списке распознанных устройств. Подробности см. в "Руководстве пользователя MFS".
- Добавить MUX Distribution: нажмите: Добавить инструмент \ выберите MUX Distrib/Inj/Rec \ выберите ваш прибор, дайте ему имя \ выберите версию MUX (здесь MUX Distribution 10) и нажмите OK для сохранения изменений. Ваш MUX должен появиться в списке распознанных устройств.
- Добавить MUX Wire: нажмите: добавить прибор \ выберите MUX Wire \ выберите ваш прибор, дайте ему имя и нажмите OK для сохранения изменений. Ваш MUX должен появиться в списке распознанных устройств.
- Откройте окна OB1, MUX Distribution и MUX Wire.
Приготовление растворов для окрашивания клеток
Совет: Идея заключается в том, чтобы сохранить все как можно более СТЕРИЛЬНЫМ. Протрите резервуары аниозимом, затем полейте водой и высушите на воздухе в BSC. Можно сделать еще один шаг, промыв аниозимом трубки, которые будут использоваться для эксперимента.
- Подготовьте резервуар с подогретой средой и подсоедините к крышке резервуара входящую в комплект трубку с наружным диаметром 1/16" и трубку катушки с наружным диаметром 6 мм. Более подробную информацию смотрите в видеоролике "Разъем для OB1". После подключения поместите среду в нагретую водяную баню.
- Повторите шаг 2 для всех водных растворов, которые вы будете использовать, а именно буфера PBS и красителя(ей).
- Подключите все трубки со спиралью диаметром 6 мм от резервуаров с растворами к внешним портам коллектора, используя резьбу 1/4''-28 и барботирующие фитинги 3/32'' OD (черные фитинги). К центральному порту распределительной системы подсоедините спиральную трубку с наружным диаметром 6 мм. Другой конец этой трубки подключите к выходу регулятора давления OB1.
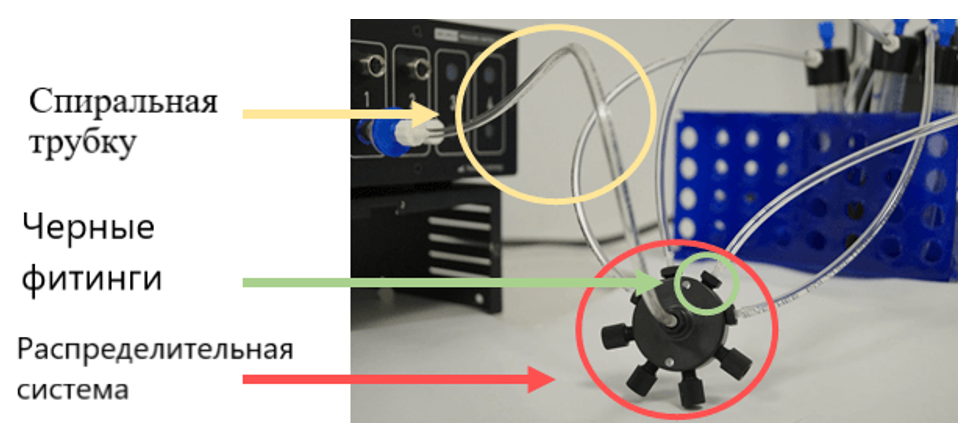
Совет: Если вы не используете все порты распределительной системы, закройте их с помощью микрофлюидных заглушек PFA 1/4''-28 с плоским дном.
Таблица длин и объемов трубок
В зависимости от установки, используемой с CO2-инкубатором и подогреваемой водяной баней, длина трубок может варьироваться в разных лабораториях. Ниже приведен рабочий спектр для записи длины трубок, расчета общего объема трубок от резервуара до микрофлюидного чипа и времени, которое потребуется для заполнения микрофлюидного чипа при требуемой скорости потока. Эта таблица также поможет определить общий объем каждого реагента, необходимого для эксперимента.
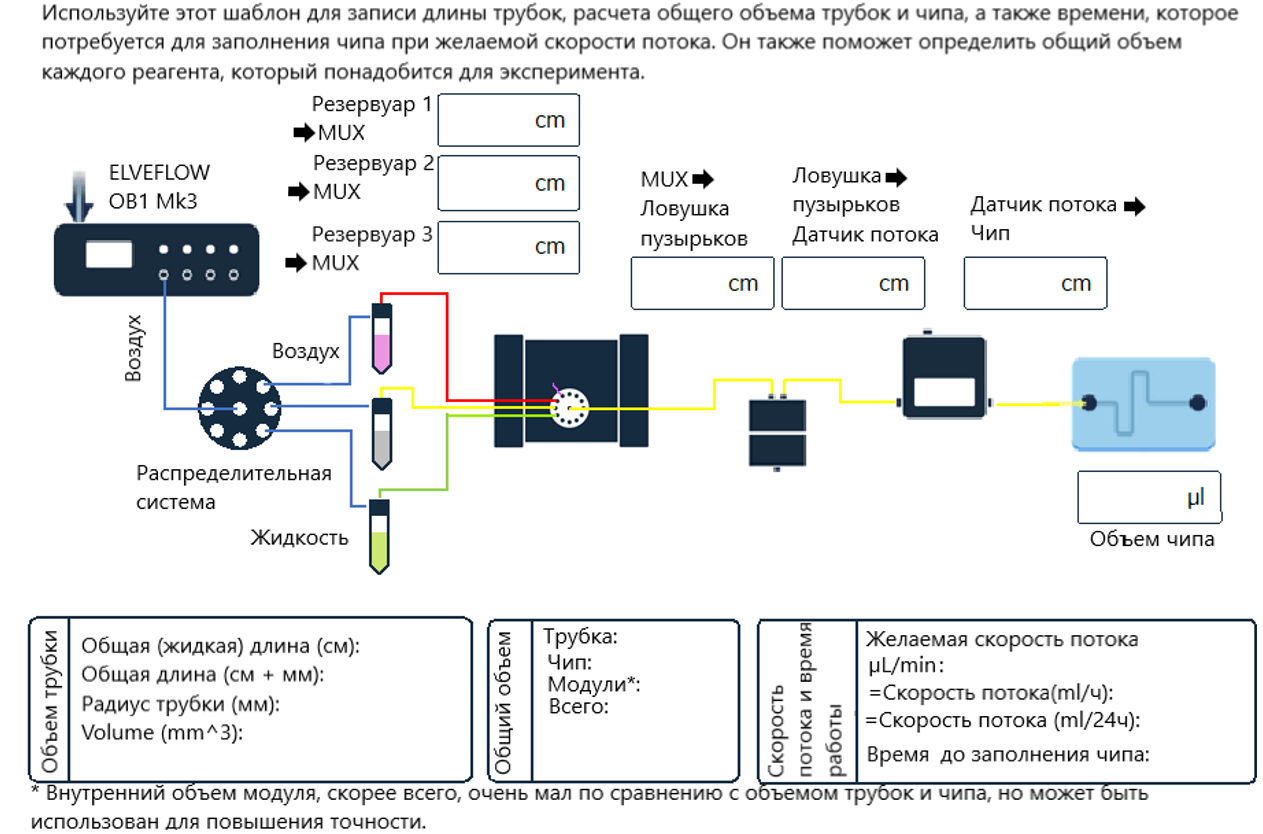
Совет: если используются светочувствительные реагенты, алюминиевую фольгу можно обернуть вокруг прозрачной трубки, чтобы минимизировать световое облучение во время эксперимента.
Совет: для экономии времени и минимизации расхода и разбавления реагента желателен небольшой общий объем трубки, что наиболее важно для расстояния между клапаном и микрофлюидным чипом. Между клапаном и микрофлюидным чипом используйте трубки с малым внутренним диаметром, например, PTFE-трубки OD 1/32.
Подготовка микрофлюидной системы для автоматического окрашивания клеток
- Подключите резервуары с растворами к входам MUX Distribution с помощью поставляемых трубок с наружным диаметром 1/16" и фитингов 1/4"-28 и добавьте тупиковый блок к одному из входов MUX Distribution. Более подробную информацию см. в "Руководстве пользователя MUX Distribution 12/1".
Совет: Подключайте растворы в порядке их введения, чтобы оптимизировать вращение клапана.
- Переименуйте резервуары в окне MUX Distribution в ПО ESI.
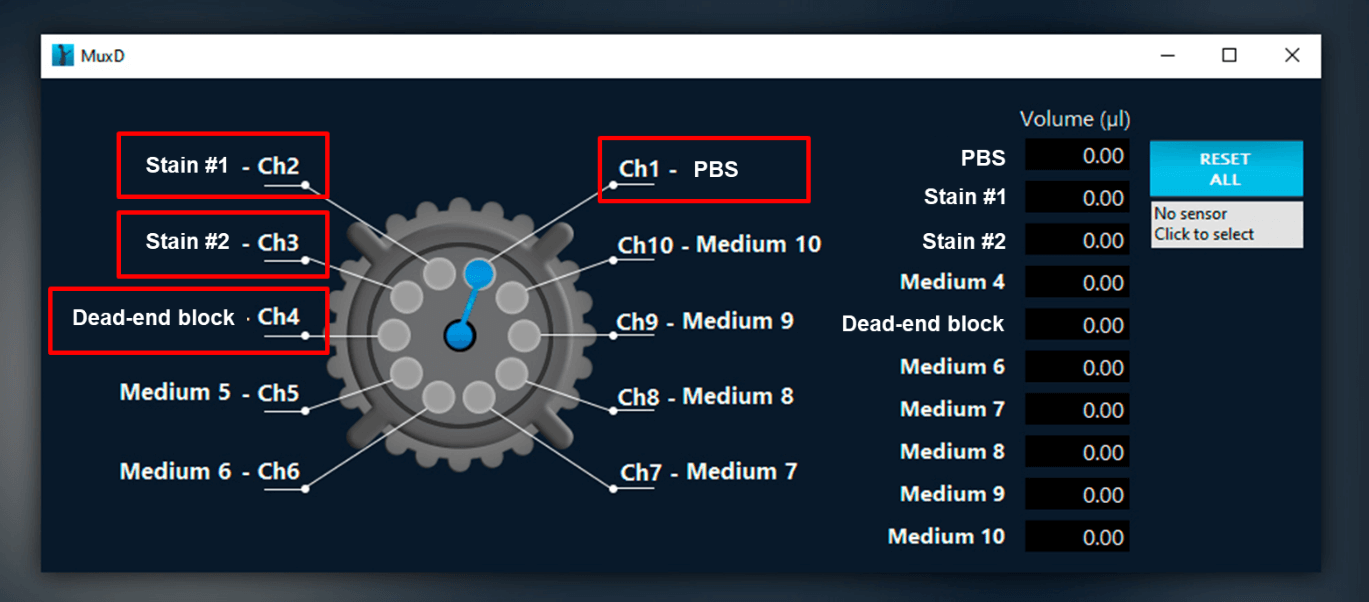
- На выходе MUX Distribution подключите один конец входящей в комплект трубки с наружным диаметром 1/16" с помощью фитинга 1/4"-28 к резервуару для отходов.
- В окне MUX Distribution выберите порт №1 (PBS) и установите давление для заполнения трубки жидкостью. Как только жидкость выйдет в отходы, воздух будет полностью удален из системы для средней линии.
- Повторите шаг 4 для всех различных подключенных к MUX Distribution устройств, выбрав соответствующий порт в окне MUX Distribution.
- После того как весь воздух будет удален из трубок с различными растворами из MUX, подсоедините трубку от выхода MUX к ловушке пузырьков. От выхода ловушки пузырьков подсоедините прилагаемую трубку с наружным диаметром 1/16" с помощью фитинга 1/4"-28 к входу датчика потока и трубку от выхода датчика потока к входу 3-ходового клапана.
Совет: Для точной настройки системы и достижения наилучшей производительности в плане регулирования расхода воздуха в систему можно добавить резистивную трубку. Более подробную информацию см. в разделе "Настройка управления расходом"
- Подсоедините трубку наружного диаметра 1/16" с помощью фитинга ¼"-28 от порта NO (нормально открытого) к емкости для отходов (это необходимо для заполнения трубки и удаления воздуха перед подключением микрофлюидного чипа, содержащего клетки). К порту NC (нормально закрытому) клапана подсоедините прилагаемую трубку с наружным диаметром 1/16" к контейнеру для отходов.

- В окне MUX Wire выберите конфигурацию NO для 3-ходового клапана. В окне MUX Distribution выберите порт №1 (PBS) и установите давление, чтобы заполнить жидкостью все трубки. Как только жидкость выйдет в отходы, воздух будет полностью удален из системы для средней линии, и вы можете установить давление на ноль.
- Теперь можно осторожно подключить микрофлюидный чип, содержащий клетки, к заполненной трубке, выходящей из порта клапана.
Совет: очень важно не вводить пузырьки воздуха в микрофлюидный чип, особенно если чип содержит небольшие каналы, так как пузырьки воздуха обычно задерживаются в чипе.
Окрашивание клеток на чипе
- Выберите порт №1 (буфер PBS) на MUX Distribution и переключите клапан в конфигурацию NO (на чип) на MUX Wire. Установите низкое давление (или скорость потока) для подачи буфера внутрь микрофлюидного чипа для промывки клеток (например, один объем чипа).
- Выберите порт №2 (пятно №1) на MUX Distribution и переключите клапан в конфигурацию NC (на отходы) на MUX Wire. Установите высокое давление (или скорость потока), чтобы протолкнуть окрашивающий раствор до клапана. Установите низкое давление (или скорость потока) и переключите клапан в конфигурацию NO (на чип) на MUX Wire. Заполните микрофлюидный чип окрашивающим раствором.
Совет: Нет необходимости заполнять всю систему драгоценным окрашивающим раствором. После короткой инъекции можно использовать PBS (или буфер по выбору), чтобы протолкнуть окрашивающий раствор из MUX Distribution в чип. Важно рассчитать или измерить время заполнения системы, чтобы оптимизировать сроки выполнения шагов с целью минимизации потерь реагентов.
- После заполнения микрофлюидного чипа остановите поток, переключившись на порт №4 (тупиковый канал) в окне MUX Distribution и установите нулевое давление (или скорость потока) в окне OB1.
Совет: Переключение на тупиковый канал вместо отключения давления предотвращает обратный поток, чтобы окрашивающий раствор оставался внутри микрофлюидного чипа.
- Инкубируйте в течение необходимого времени.
- Повторите предыдущие четыре шага для всех различных окрашиваний, необходимых для эксперимента.
- Выберите порт №1 (буфер PBS) и установите давление (или скорость потока) для подачи буфера внутрь микрофлюидного чипа для промывки клеток.
- Выберите порт №4 (тупиковый канал) в окне MUX Distribution и установите нулевое давление (или скорость потока) в окне OB1.
- Клетки внутри микрофлюидного чипа готовы к визуализации под микроскопом.
Общая очистка оборудования для окрашивания клеток
- Тщательно промойте трубки и модули водой, затем аниозимом (1%). Сделайте окончательную промывку этанолом и высушите воздухом (воздух выпустите из пустого резервуара).
- Меняйте жидкостные трубки между экспериментами и используйте стерильные резервуары для новых экспериментов. Периодически заменяйте мембрану ловушки пузырьков
Автоматизированное окрашивание клеток
Для автоматизации управления потоком и переключения жидкостей при окрашивании клеток можно выполнить следующие действия.
- Чтобы создать последовательность, нажмите на верхнюю среднюю кнопку "Create Sequence" в главном окне программы ESI: появится новое окно.
- Вернитесь к окну OB1: установите желаемую скорость потока или давление для вашего эксперимента и сохраните конфигурацию, нажав на кнопку "Config". Повторите для всех значений расхода или давления, которые будут использоваться в ходе эксперимента. Не забудьте сохранить конфигурацию давления или расхода "0". Для получения более подробной информации обратитесь к "Руководству пользователя ESI".
- Аналогично, в окне MUX Wire: сохраните конфигурации для каждого положения клапана, NC (нормально закрытый) и NO (нормально открытый), нажав на "Config".
Совет: Автоматизированный захват и окрашивание клеток следует проводить с использованием клапанов микрофлюидики, чтобы избежать потери реагентов и засорения системы.
- Вернитесь к окну последовательности: в левой части окна нажмите на зеленое поле "OB1" (в средней части появится строка "OB1: Select instrument"), в правой части выберите прибор (ваш контроллер потока OB1 должен появиться при нажатии на "Instrument") и загрузите конфигурацию, сохраненную ранее.
- В левой части окна последовательности нажмите на фиолетовое поле "DIST" (появится новая строка "DIST: Select Instrument"): выберите ваш прибор и напишите в поле "Valve position" номер нужного порта, соответствующего необходимому раствору.
Совет: Вы также можете выбрать тип вращения MUX Distribution для вашего удобства (кратчайший, по часовой стрелке или против часовой стрелки).
- В левой части окна последовательности нажмите на фиолетовое поле "MUX" (появится новая строка "MUX: Select Instrument"): выберите свой прибор и загрузите конфигурацию клапана, соответствующую необходимому решению (нормально закрытый или нормально открытый).
- В левой части окна последовательности нажмите на поле "Clock" (появится новая строка с временной рамкой): установите желаемую продолжительность.
- Создайте последовательность впрыска жидкости в соответствии с процедурами, описанными в шаге 4-7.
- Вариант: в левой части окна последовательности нажмите на поле "GO". Этот шаг позволит вам повторить последовательность: выберите "целевой шаг" (2, если вы хотите повторить всю последовательность без изменения конфигурации OB1) и "время" - сколько раз вы хотите ее повторить.
- В левой части окна последовательности нажмите на синее поле "END" (появится новая строка "END"). Это означает, что ваша последовательность закончена.
- Ниже приведен пример последовательности для окрашивания клеток двумя красителями:
a) Промойте клетки PBS.
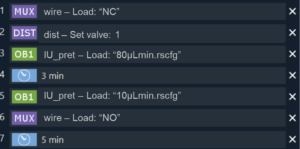
b) Залейте чип красителем №1 и инкубируйте в течение 30 мин.

c) Повторите шаг (a), чтобы промыть клетки PBS.
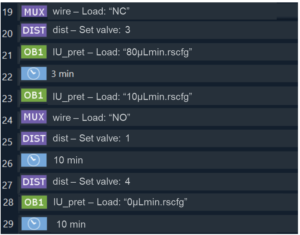
d) Заполните чип красителем №2 и инкубируйте в течение 30 мин.
e) Повторите шаг (а), чтобы промыть клетки PBS.
f) Чип готов к визуализации.
Результаты
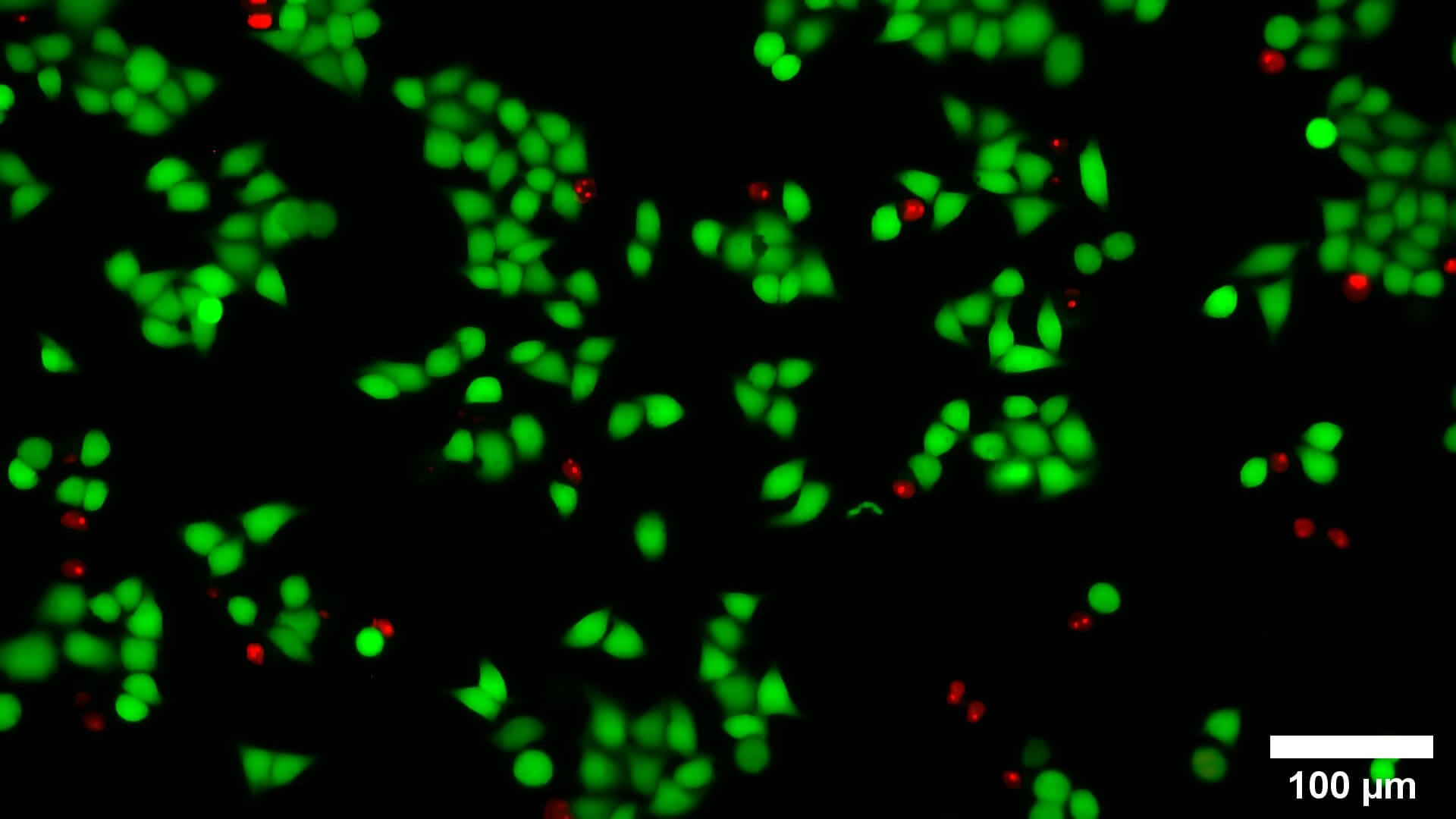
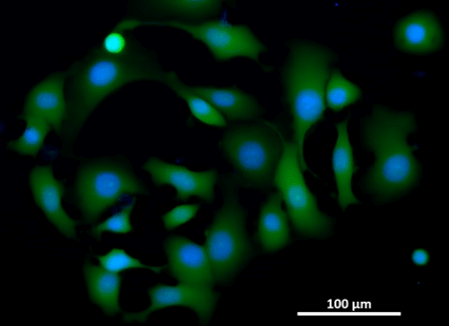
LIVE/DEAD окрашивание клеток HeLa (кальцеин AM и йодистый пропидий, объединенное изображение)
Этот протокол может быть адаптирован с клетками MCF7
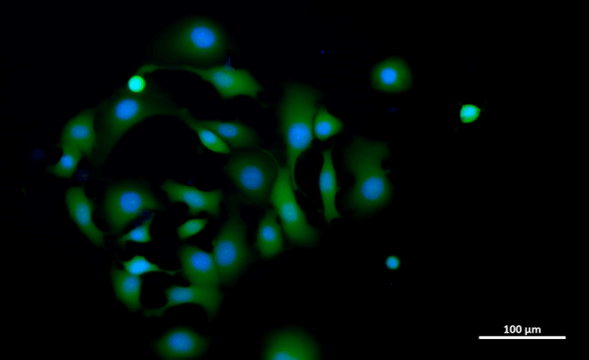
Окрашивание живых клеток MCF7 (кальцеин AM/ Hoechst 33342, объединенное изображение)
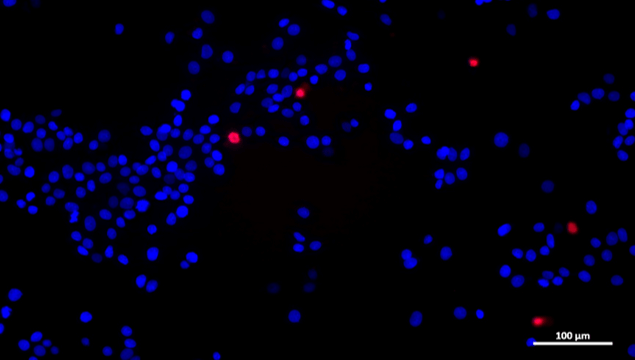
LIVE/DEAD окрашивание клеток MCF7 (Hoechst 33342 и йодид натрия, объединенное изображение)