В центре внимания нейробиологических исследований находится ответ на вопросы о развитии, организации и функционировании нервной системы. Микроскопия - ценный инструмент для выявления сложности нейронных сетей, позволяя получить структурное и механистическое представление на молекулярном и клеточном уровне. За последнее десятилетие достижения в области методов визуализации и маркировки позволили различать структуры и процессы с высоким пространственно-временным разрешением даже в живых клетках.
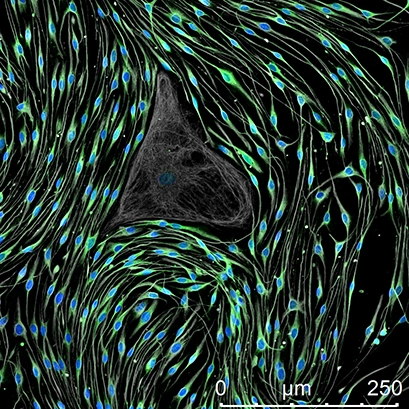
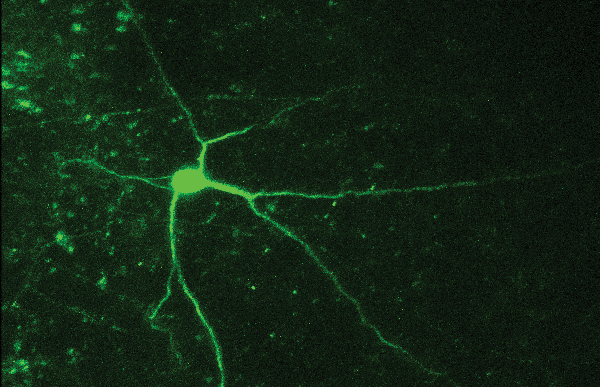
Фибробласт крысы, окруженный параллельно выровненными крысиными шванновскими клетками (SCs), культивировали в 8-луночном µ-Slide ibidi и окрашивали на SC-маркер S100 (зеленый), виментин (серый) и DAPI (синий). Изображение получено с помощью лазерного сканирующего микроскопа. Предоставлено: Флавия Миллези, Медицинский университет Вены, Австрия
Визуализация субклеточных структур и компонентов
Флуоресцентная маркировка
Флуоресцентное маркировка является широко используемым и простым в применении методом выявления субклеточных структур и компонентов, а также их партнеров по взаимодействию в основном в фиксированных клетках или тканях. Метки включают отдельные частицы (например, квантовые точки или оригами, меченные красителем), органические красители (например, красители родамина или Alexa) и флуоресцентно меченные антитела. Например, Шаарвари Бхат и др. (Институт Пастера, Париж, Франция) визуализировали актиновые структуры нейронов CAD (Cath.a-дифференцированных) клеток с помощью родамина фаллоидина, что позволило обнаружить и количественно определить туннелирующие нанотрубки, связанные клетки (TNT).
Чтобы одновременно визуализировать и охарактеризовать несколько клеточных компонентов в одном и том же биологическом образце, часто используется подход иммуномечения с использованием разных первичных и вторичных антител. Например, Флавия Миллези и др. (Венский медицинский университет) разработали панели многоцветного окрашивания путем экспрессии специфических маркеров для различения шванновских клеток, фибробластов и нейронов ганглия задних корешков в одной и той же клеточной культуре. Иммуноокрашивание можно также проводить на целых тканях (иммуногистология). Для количественной оценки нейронов ствола мозга Джованни Уссеглио и др. (Институт неврологии Париж-Сакле, Франция) препарировали мозг взрослых мышей, затем фиксировали, замораживали и делали срезы перед иммуноокрашиванием.
Эндогенная маркировка живых клеток
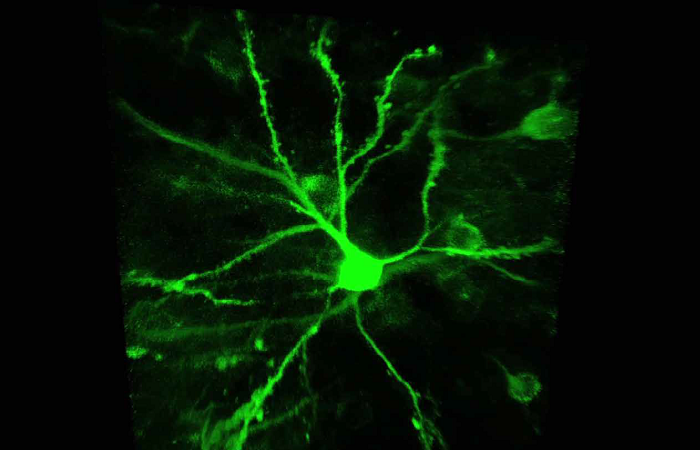
В частности, для экспериментов по визуализации живых клеток требуется правильный подход к маркировке, который не мешает жизнеспособности клеток и их функциям. Для этого подхода можно использовать низкомолекулярные связующие (например, SiR-actin или LifeAct), связанные с флуоресцентным белком (например, GFP или RFP). LifeAct окрашивает структуры филаментного актина (F-актина) в живых (или фиксированных) эукариотических клетках и тканях. Например, LifeAct, помеченный RFP, использовался для визуализации F-актинового цитоскелета для анализа дендритных шипиков в живых первичных нейронах гиппокампа.
Визуализация трехмерных нейронных совместных культур
При имитации сложной микросреды живой ткани важно исследовать интересующие клетки, а также любые другие клетки, с которыми они взаимодействуют в окружающем клеточном матриксе. Таким образом, создание 3D-моделей совместных культур этих взаимодействующих клеток в пределах физиологического каркаса является важной стратегией для понимания клеточной структуры и функции.
Чтобы изучить взаимодействие периферических сенсорных нейронов (ПСН) и эндотелиальных клеток (ЭК) человека, а также выяснить, влияют ли ПСН на ангиогенез, Сатья Каннан и др. (Факультет стоматологии, Национальный университет Сингапура, Сингапур) разработали систему трехмерного совместного культивирования, состоящую из эмбриональных стволовых клеток человека (hESC) PSN и эндотелиальных клеток hESC, встроенных в матрицу из коллагена 1 типа.
Флавия Миллези и др. (Венский медицинский университет) выполнили визуализацию живых клеток и ручное отслеживание совместной культуры фибробластов и шванновских клеток, чтобы выяснить, влияют ли крысиные фибробласты на миграционное поведение крысиных шванновских клеток, культивируемых на регенеративном шелке пауков.
Анализ функции и организации нейронных клеток с использованием высокого пространственно-временного разрешения
Визуализация живых клеток
Визуализация живых нейронных клеток и тканей помогает получить представление о механизмах нейронных процессов и функций. Например, флуоресцентная визуализирующая микроскопия жизни (FLIM) в срезах мозга показала, что метаболические изменения были причиной митохондриальной дисфункции при нейродегенеративных заболеваниях.
Физиологические условия
В частности, для долгосрочной визуализации живых клеток крайне важно поддерживать физиологические условия, контролируя температуру, pH, кислород и влажность. Например, визуализация живых клеток нейронов центральной нервной системы (ЦНС) при стабильных условиях окружающей среды 37°C и 5% кислорода позволила визуализировать поляризацию и удлинение аксонов в 3D в течение 48 часов. Нейроны ЦНС были встроены в коллагеновые гидрогели, а затем визуализированы с помощью дифференциально-интерференционной контрастной (ДИК) микроскопии в физиологических условиях, чтобы показать, что поведение роста аксонов в 3D является амебоидным и не зависит от спаек.
Чтобы смоделировать физиологические условия для эндотелиальных клеток, таких как эндотелиальные клетки микрососудов головного мозга in vitro, крайне важно культивировать их в определенных условиях напряжения сдвига с непрерывным потоком среды. Например, Цзин-Цюань Гао и др. (Отделение сестринского дела, Харбинский медицинский университет, Дацин, Дацин, Китай) показали, что изменение церебрального кровотока в мозге песчанок после глобальных церебральных ИР влияет на функцию микрососудистого эндотелия и нейронов.
Визуализация нейронных клеток со сверхвысоким разрешением
В нервной системе многие нейронные структуры и процессы меньше предела разрешения света. Поэтому трудно получить изображение деталей, которые меньше или приблизительно равны 200 нм, вместе с обычными методами световой микроскопии. Развитие методов сверхвысокого разрешения, таких как микроскопия структурированного освещения (SIM), микроскопия на основе подавления спонтанного испускания (STED) или фотоактивированная локализационная микроскопия (PALM), позволило преодолеть дифракционный барьер света и, следовательно, можно визуализировать такие маленькие компоненты, как синаптические пузырьки размером 40 нм. Например, Лука Колнаги и др. (Кафедра молекулярной биохимии и фармакологии, Институт фармакологических исследований Марио Негри, Милан, Италия) смогли впервые локализовать отдельные белки SENP в культивируемых первичных нейронах гиппокампа с помощью микроскопии структурированного освещения (SIM).
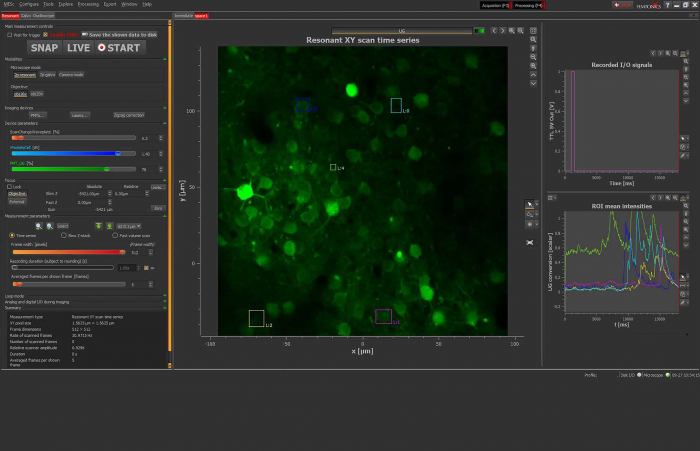
Визуализация кальция в нейронах
Передача сигналов кальция играет ключевую роль почти во всех клеточных задачах. В нейронах, например, ионы Ca2+ ответственны за высвобождение нейротрансмиттеров из синаптических пузырьков. Визуализация кальция позволяет контролировать электрическую активность нейронов, отслеживая поток Са2+ с помощью флуоресцентных зондов, которые активируются при связывании Са2+. Кальций-визуализация может использоваться в качестве инструмента для оценки функциональности клеток, например, при дифференциации индуцированных человеком плюрипотентных стволовых клеток (ИПСК) в нейроны.