Биологический контекст
Эндоплазматический ретикулум (ЭР) - это мембраносвязанная органелла, расположенная в цитоплазме всех эукариотических клеток. ЭР играет центральную роль во многих биологических процессах, включая синтез белка, метаболизм глюкозы и липидов, сигнализацию и динамику кальция (Öztürk et al, 2020). Эта богатая структура формируется и поддерживается постоянным процессом ремоделирования, который включает синтез, перенос и слияние с уже существующими канальцами ЭР. Дисфункция ЭР может вызывать тяжелые заболевания, такие как нейродегенеративные заболевания, рак или болезни обмена веществ (Ozcan & Tabas, 2012; Roussel et al, 2013; Oakes, 2020). Таким образом, визуализация динамики ЭР в реальном времени стала золотым стандартом для лучшего понимания соответствующих патофизиологических путей.
Техника FRAP для визуализации живых клеток
При визуализации живых клеток биологи обычно используют флуоресцентные маркеры для отслеживания органелл и/или белков. Однако эти флуорофоры могут навсегда утратить способность излучать флуоресценцию, если возбуждающий свет очень интенсивный или время экспозиции слишком велико. Это необратимое явление называется фотообесцвечиванием. Такая потеря сигнала является реальной проблемой в большинстве экспериментов по визуализации, за исключением некоторых методов, которые используют преимущества этого изменения, например, FRAP (восстановление флуоресценции после фотообесцвечивания). В 1970-х годах эксперименты FRAP стали новым инструментом для изучения подвижности и динамики флуоресцентных белков в живых клетках (Axelrod et al, 1976). В настоящее время он стал распространенным методом для изучения динамики практически во всех аспектах клеточной биологии, таких как динамика цитоскелета (Appaduray et al, 2016), транспорт внутриклеточных везикул (Tagawa et al, 2005), клеточная адгезия (von Wichert, 2003), митоз (Raccaud et al, 2019) или трансдукция сигналов (Giese et al, 2003). Вкратце, флуоресцентные молекулы необратимо фотообесцвечиваются в интересующих областях (ROI) клетки (цитоплазма, мембрана, ...) мощным сфокусированным лазерным лучом, удаляя все флуоресцентные сигналы (рис. 1A). Последующая диффузия окружающих неотбеленных флуоресцентных молекул в отбеленную область приводит к восстановлению флуоресценции (Kang et al, 2010; Lippincott-Schwartz et al, 2018).
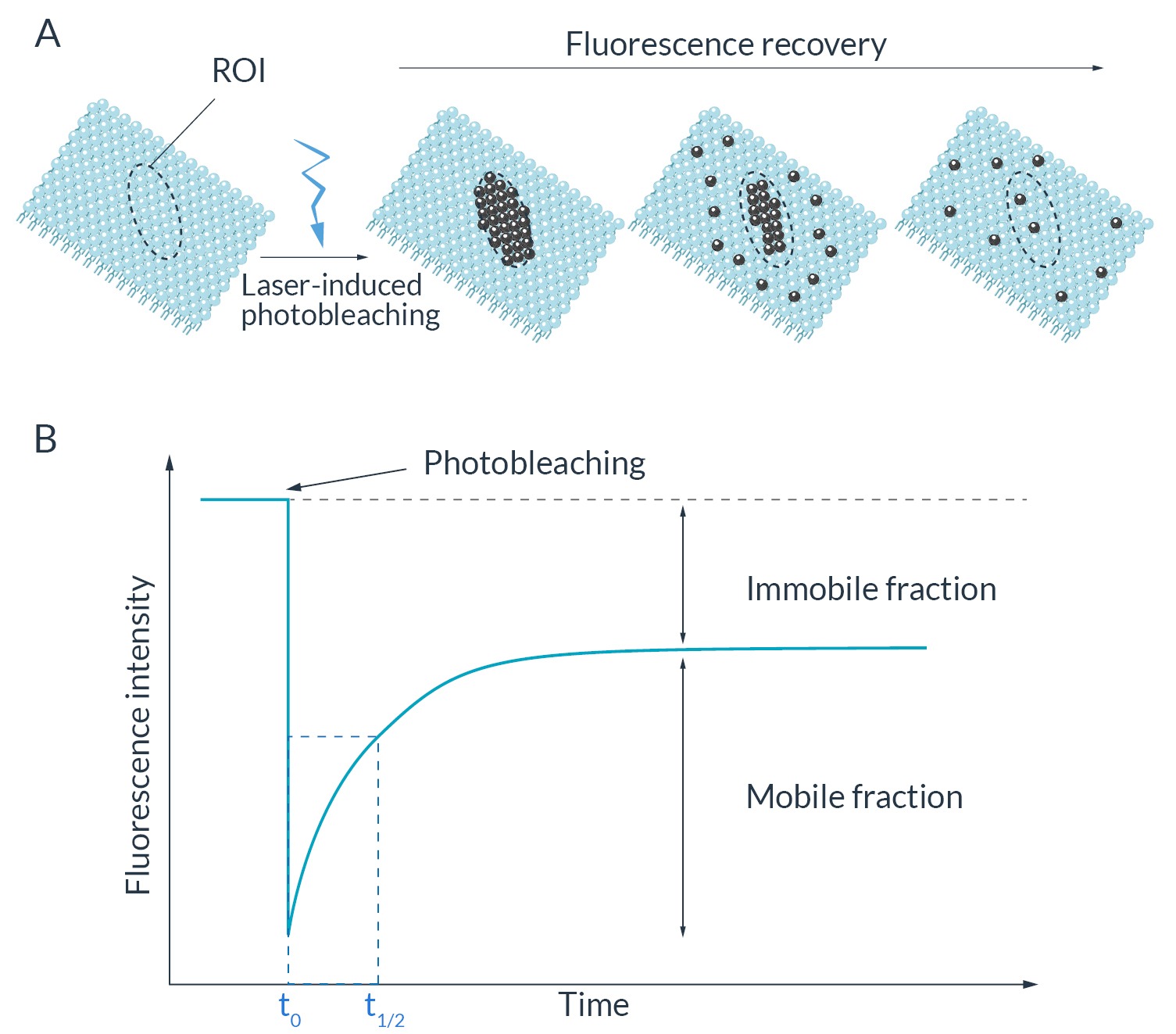
Рисунок 1. Принцип визуализации FRAP
(A) Перед лазерно-индуцированным фотообесцвечиванием флуоресцентные белки равномерно распределены в мембране. Сразу после фотообесцвечивания все зонды, расположенные в областях интереса (ROI), больше не способны излучать флуоресценцию. Возвращение флуоресценции происходит только за счет обмена нефлуоресцентных и флуоресцентных белков путем латеральной диффузии внутри мембраны. (B) Схематическая кривая, показывающая восстановление флуоресценции во времени после фотообесцвечивания. Неподвижная фракция - это разница между начальной и конечной интенсивностью флуоресценции. Она представляет собой часть флуоресцентного белка, который не способен перемещаться внутри наблюдаемого биологического образца. Время полувосстановления соответствует времени, необходимому для достижения 50% от конечной интенсивности флуоресценции (t1/2) после обесцвечивания (t0).
Для характеристики динамики этих флуоресцентных белков можно измерить некоторые параметры. Одним из них является время восстановления (t1/2), которое соответствует времени от момента отбеливания (t0) до момента, когда интенсивность флуоресценции достигла половины от конечной восстановленной интенсивности (t1/2). Чем короче время полураспада, тем быстрее происходит восстановление флуоресценции и тем выше диффузия. Подвижность флуоресцентных белков также можно оценить по профилю кривой восстановления интенсивности (Ishikawa-Ankerhold et al, 2012). Подвижные и неподвижные фракции могут быть измерены путем расчета соотношения конечной и начальной интенсивности флуоресценции (рис. 1B).
Для проведения экспериментов FRAP необходимо отметить, что система должна быть адаптирована к каждому эксперименту. Например, восстановление флуоресценции может быть очень быстрым и требует систем визуализации с высокой частотой кадров для улучшения временного разрешения эксперимента. Управление лазером - еще один ключевой параметр, позволяющий исследователям адаптировать, персонализировать и оптимизировать выбор ROI.
Лазеры Oxxius для экспериментов по фотоманипуляции
INSCOPER (Кессон-Севинье, Франция) уже несколько лет сотрудничает с разработчиком и производителем лазерных источников Oxxius (Ланнион, Франция). Эта компания разработала передовые лазерные модули непрерывной волны для широкого спектра применений в биофотонике, спектроскопии, метрологии и др. Oxxius выпускает комбинаторы L4Cc и L6Cc, которые являются самыми компактными многоцветными лазерными источниками "все в одном", которые могут включать соответственно до 4 или 6 длин волн, передаваемых по 4 различным выходам оптического волокна. Каждый лазер может модулироваться аналоговыми и цифровыми входами. Эти контроллеры могут обеспечить большую панель длин волн от 375 до 1064 нм. Модули расширения повышают гибкость комбинатора за счет интеграции быстро переключаемых выходных портов для FRAP, регулируемой мощности разделения для микроскопии светового листа и других расширенных функций.
Решение Inscoper для визуализации FRAP
Основанная на технологии гальванометрических зеркал, система Inscoper scanFRAP представляет собой комплексное решение для микроскопии для экспериментов по фотоманипуляции и оптогенетике. Продукт состоит из программно-аппаратного комплекса, совместимого с современными видеомикроскопами, используемыми в биологических науках. Включая специально разработанный электронный блок для управления стойкой микроскопа и сторонними устройствами, Inscoper scanFRAP обеспечивает новый пользовательский опыт для приложений фотоманипуляции с улучшенными техническими характеристиками, полной системной интеграцией и простотой использования. Ядро технологии Inscoper устраняет любые программные задержки при управлении всей системой микроскопии. Это увеличивает временное разрешение по сравнению с традиционными подходами, что является основным преимуществом для применения в визуализации живых клеток (рис. 2). Исследователи имеют полный контроль над всеми настройками лазера (мощность, плотность точек, время импульса). Они могут полностью персонализировать и оптимизировать обесцвеченные области, модулируя область интереса (ROI) в пользовательском интерфейсе программного обеспечения.
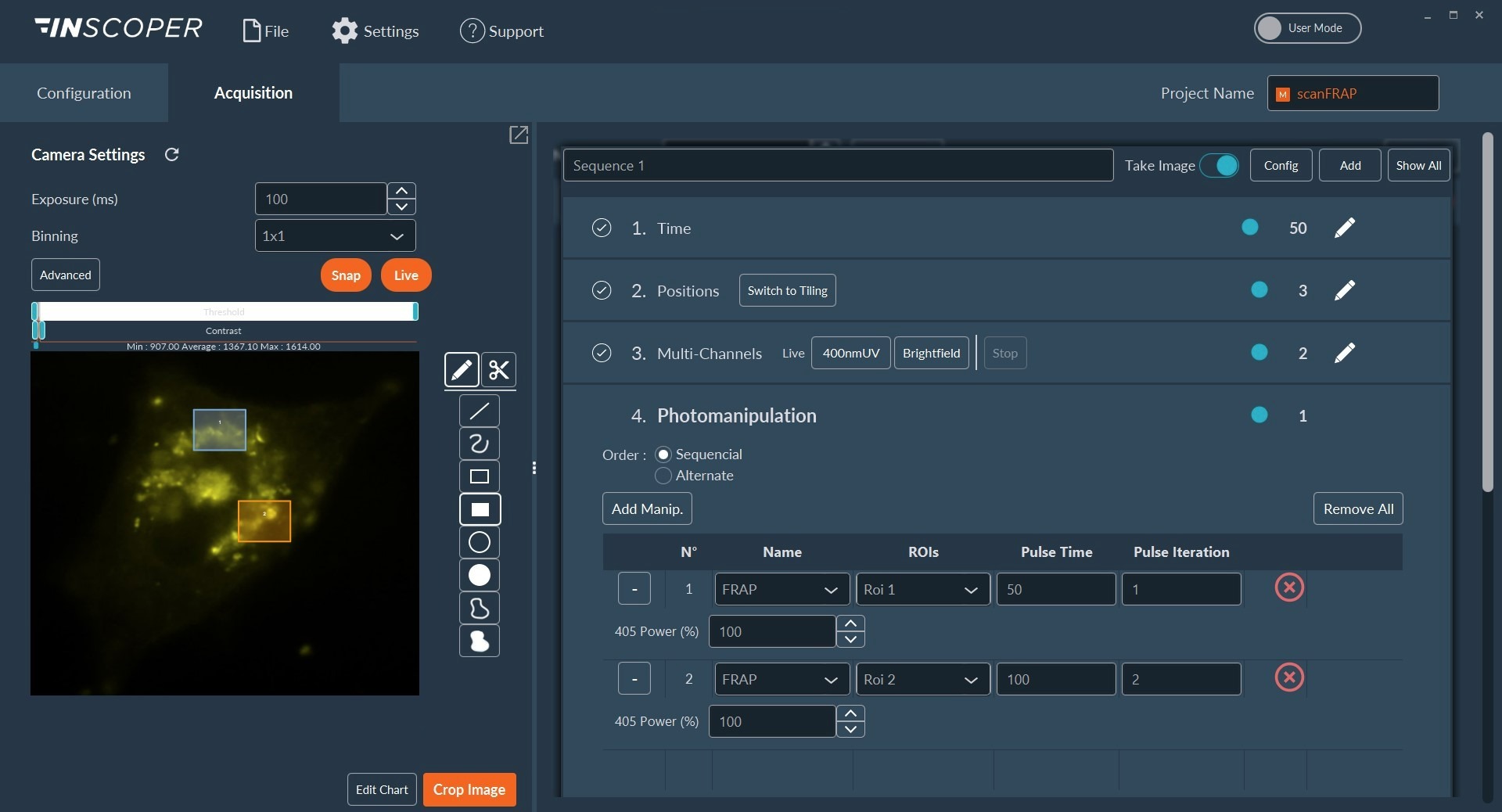
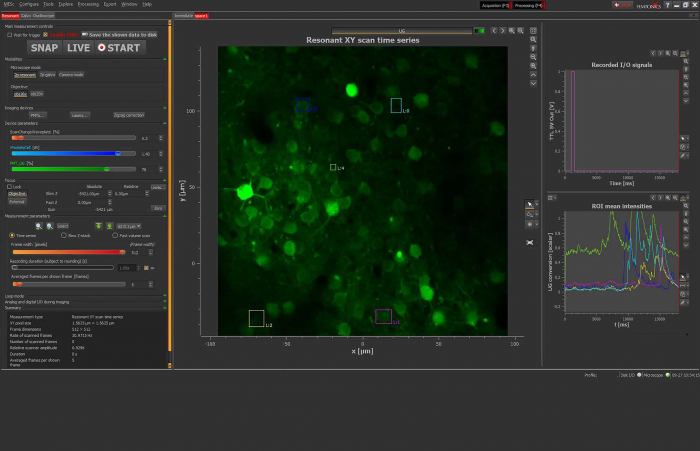
Рисунок 2: Интерфейс программного обеспечения Inscoper
Обзор программного обеспечения Inscoper, используемого для управления последовательностью сбора данных с многомерными параметрами, включая таймлапс, мультипозицию, многоканальность и фотоманипуляцию. Все эти параметры полностью настраиваются, чтобы быть более подходящими для экспериментов пользователя.
Эксперименты с FRAP
Цели
Цель экспериментов охарактеризовать динамику эндоплазматического ретикулума в живых клетках с помощью метода FRAP.
Материал
Использовался микроскоп Nikon Ti2 Eclipse (Nikon, Токио, Япония) с объективом Plan Apo λ 60x 1.4 NA с масляной иммерсией (MRD01605; Nikon). Для этого эксперимента камера была цифровой CMOS ORCA-Fusion BT (C15440-20UP; Hamamatsu Photonics, Hamamatsu, Япония), а источник света был от CoolLED (pE-800fura; CoolLED, Andover, Великобритания). Видеомикроскопию и FRAP проводили с помощью Inscoper scanFRAP (INSCOPER, Кессон-Севинье, Франция) с источником лазерного излучения 405 нм (L6Cc; Oxxius, Ланнион, Франция). Все изображения были деконволюционированы с помощью программного обеспечения Microvolution (Microvolution, Купертино, Калифорния, США).
Метод
Клетки HeLa были трансфицированы для сверхэкспрессии YFP (желтого флуоресцентного белка) в их эндоплазматическом ретикулуме. Для эксперимента FRAP определяли ROI и обесцвечивали с помощью 405-нм лазера живые клетки и фиксированные клетки в качестве отрицательного контроля. Затем измерялось восстановление флуоресценции. Эксперименты FRAP в основном состоят из трех этапов. Сначала снимается короткий временной интервал до отбеливания, чтобы получить базальный уровень флуоресценции. В данном случае стабильный и сильный сигнал YFP наблюдался в трансфецированных клетках до фотоманипуляции. Затем выбирается область интереса (ROI) и фотообесцвечивается с соответствующими настройками лазера (длина волны, интенсивность, плотность точек, ...). Наконец, выполняется еще один таймлапс для наблюдения в реальном времени за восстановлением флуоресценции в обесцвеченной области интереса.
Результаты
Лазерное микрооблучение представляет собой мощный инструмент для мониторинга репарации ДНК с высоким временным и пространственным разрешением. Повреждения ДНК индуцировались в области интереса (ROI), предварительно определенной с помощью программного обеспечения Inscoper. Во время получения данных можно было наблюдать постепенный набор белка ALC1-GFP по всей длине ROI (рис. 3A). Затем была измерена средняя интенсивность флуоресцентного сигнала на поврежденном участке. В качестве контроля также измерялся сигнал от неизмененной ROI. В облученной области наблюдалось быстрое увеличение сигнала, который оставался стабильным менее 10 секунд (Рисунок 3B). Напротив, интенсивность сигнала в контрольной области немного снизилась после фотоманипуляции. Накопление ALC1-GFP также можно охарактеризовать по ширине полосы (Рисунок 3C). В данном эксперименте это явление происходило быстро с половинным временем 47,7 ± 7,1 секунды и полным восстановлением чуть более чем за 300 секунд (Рисунок 3D). YFP-меченые белки из ЭР в живых клетках оказались подвижными и способными быстро диффундировать внутрь цитоплазмы клетки.
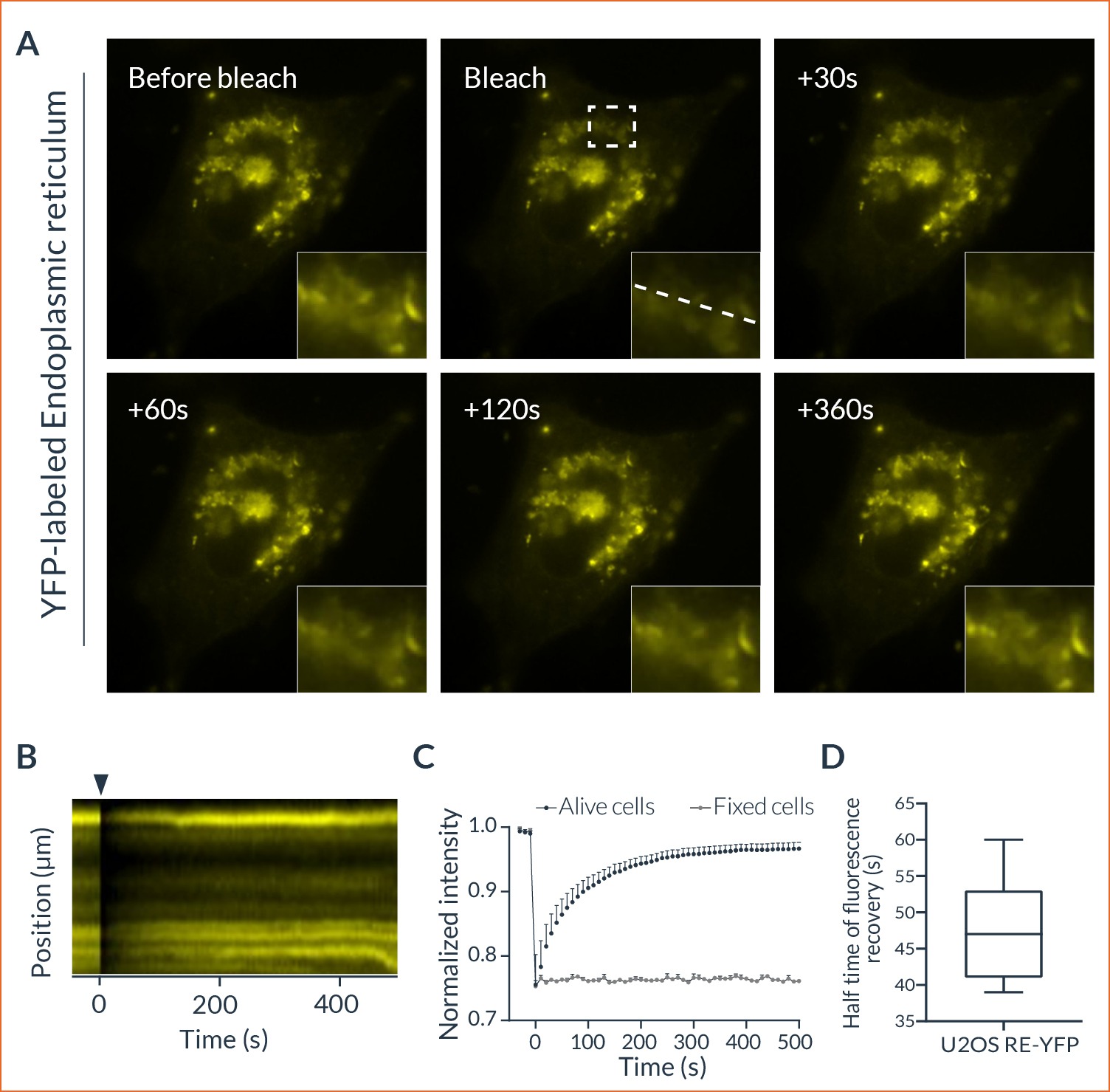
Рисунок 3: Эксперимент FRAP для мониторинга динамики эндоплазматического ретикулума в живых клетках
(A) Репрезентативный пример клеток HeLa, экспрессирующих YFP-ER, до и после фотообесцвечивания. Восстановление флуоресцентного сигнала после фотообесцвечивания в области, обозначенной пунктирным прямоугольником, визуализируется с течением времени. Эта область увеличена в правом нижнем углу каждого изображения. Представленная пунктирная линия указывает на область, используемую для следующей кимограммы. (B) Кимограмма, представляющая эволюцию интенсивности флуоресценции в зависимости от времени. Черный наконечник стрелки обозначает событие фотообесцвечивания. (C) Нормализованная количественная оценка восстановления флуоресценции после фотообесцвечивания (n = 7). Данные выражены как среднее ± SEM. (D) Время полувосстановления флуоресценции в анализах FRAP (n = 7).
Важно отметить, что подход FRAP — не единственный метод, доступный для характеристики динамики ЭР. Его также можно контролировать с помощью видеомикроскопии (рис. 4). Здесь была визуализирована трубочка ER, что дало пользователям возможность измерить ее движение и ремоделирование. Эта информация дополняет информацию, полученную ранее с помощью FRAP, и дает информацию о формировании, слиянии/делении этих сложных органелл.
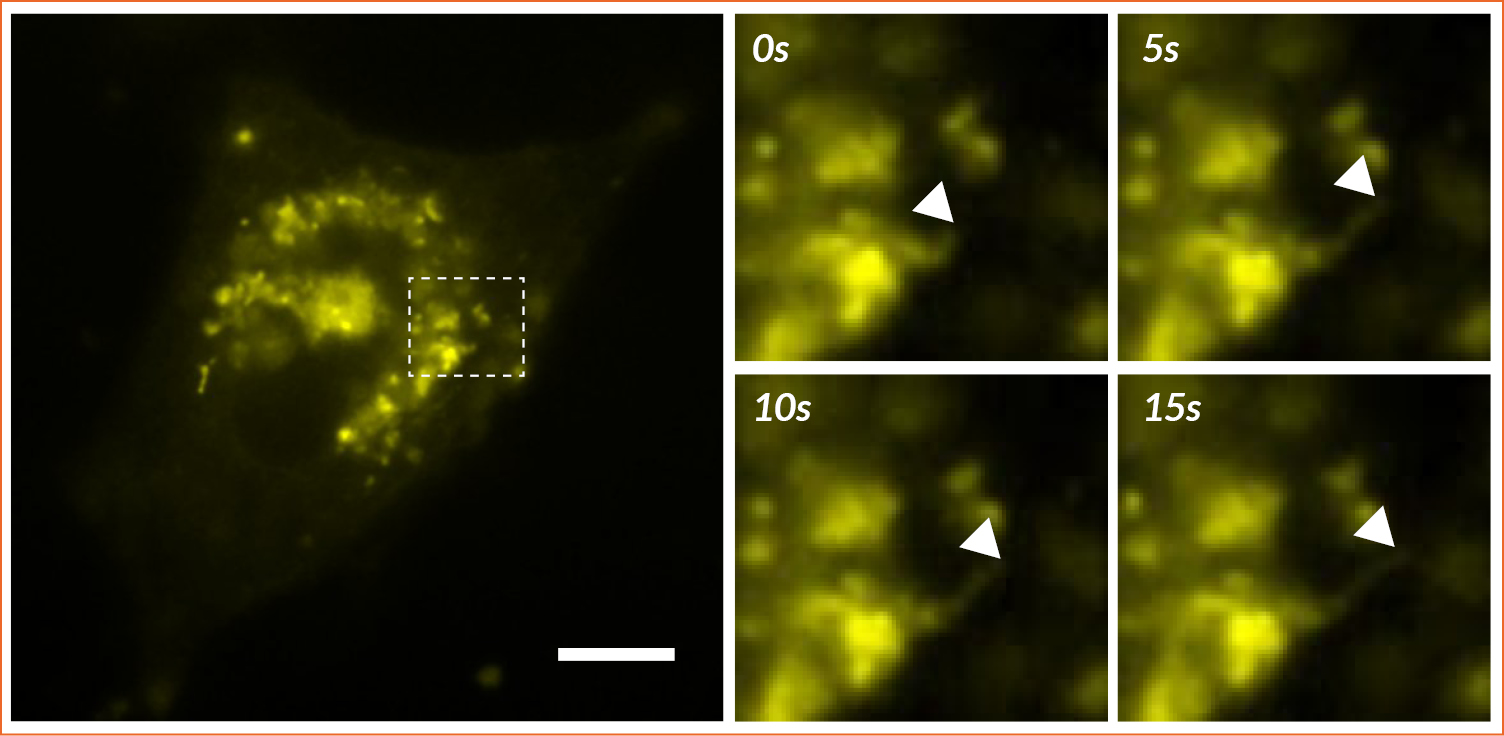
Рисунок 4: Мониторинг динамики канальцев эндоплазматического ретикулума
Широкопольная флуоресцентная визуализация клеток HeLa, трансфицированных YFP-ER. Заштрихованный прямоугольник увеличен в правой части рисунка. Удлинение канальца ER отмечено стрелкой на изображениях. Масштабная линейка = 10 мкм.
Резюме
Эксперименты FRAP с использованием Inscoper scanFRAP дают биологам и пользователям микроскопов возможность характеризовать в реальном времени кинетику флуоресцентно-меченых белков, сочетая фотоманипуляцию и видеомикроскопию с высоким пространственно-временным разрешением. ScanFRAP отличается от других продуктов своими настраиваемыми функциями и плавной интеграцией в универсальное и удобное программное решение для получения изображений. В сочетании с лазерами Oxxius это идеальное решение для исследования движения/диффузии белков, компартментализации и связей между внутриклеточными компартментами, скорости белкового обмена между компартментами и характеристик связывания между белками. Стоит отметить, что Inscoper scanFRAP можно комбинировать с другими передовыми методами световой визуализации (FLIM, FRET) или с различными модальностями освещения (вращающийся диск, TIRF, HiLo, световой лист…), чтобы получить дополнительный подход.