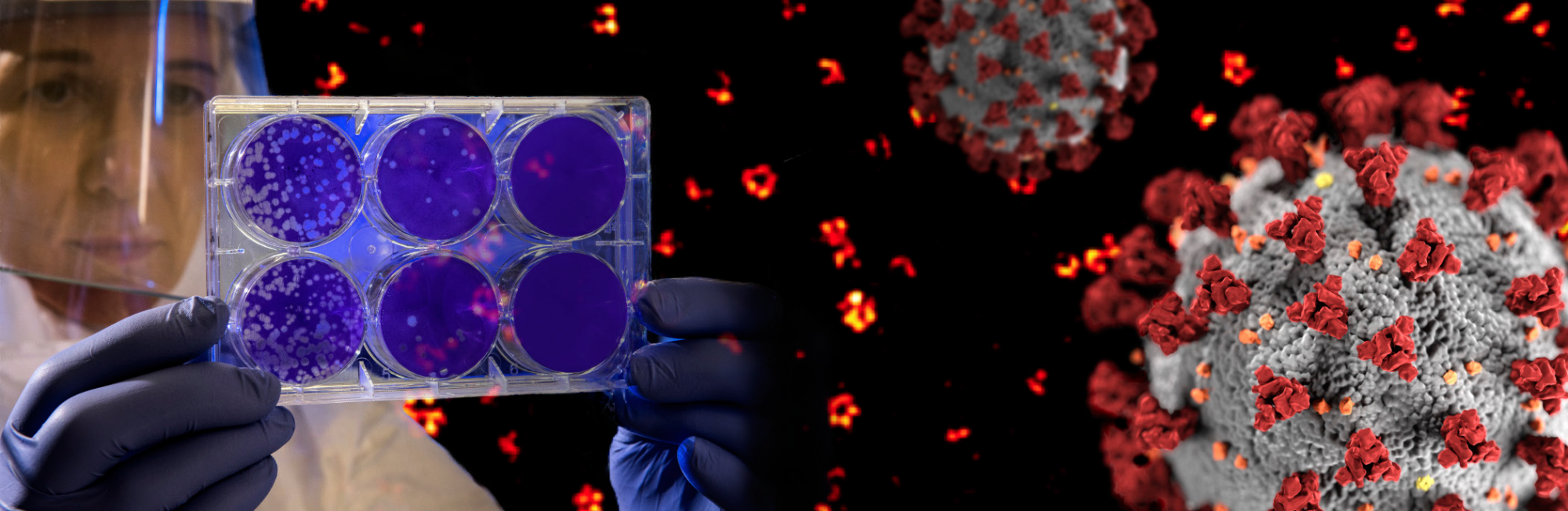
Микроскопия сверхвысокого разрешения – это широко используемый метод исследования биологических особенностей образцов за пределами дифракционного предела, таких как ядерные поры, покрытые клатрином везикулы, периодичность актинового скелета в нейронах и вирусы. В этой статье будет рассказано о преимуществах STED микроскопии и её вкладе в область вирусологии. Авторы статьи расскажут о достижениях в исследованиях вирусов, которые стали возможными благодаря STED микроскопии, и сделают предположение, в каком направлении данные исследования могут пойти.
Вирусные частицы различаются по размеру в зависимости от видов вирусов. Один из самых маленьких вирусов, парвовирус, имеет размер около 20 нм, в то время как самые крупные известные вирусные частицы семейства мимивирусов обладают размером капсида до 500 нм, что уже сравнимо с размером бактерии (рис. 1). Таким образом, благодаря своим размерам вирусные частицы и их субструктуры могут быть детально изучены с помощью методов микроскопии со сверхвысоким разрешением, таких как STED или методы одномолекулярной локализации, которые обеспечивают разрешающую способность около 20 нм. Многочисленные исследования с использованием методов визуализации со сверхразрешением уже расширили научные знания о вирусе иммунодефицита человека (ВИЧ-1), вирусе гриппа A, вирусе простого герпеса (HSV), респираторно-синцитиальном вирусе (RSV), вируса осповакцины, аденоассоциированном вирусе (AAV), вирусе Нипах (Niv), аденовирусе и многих других.
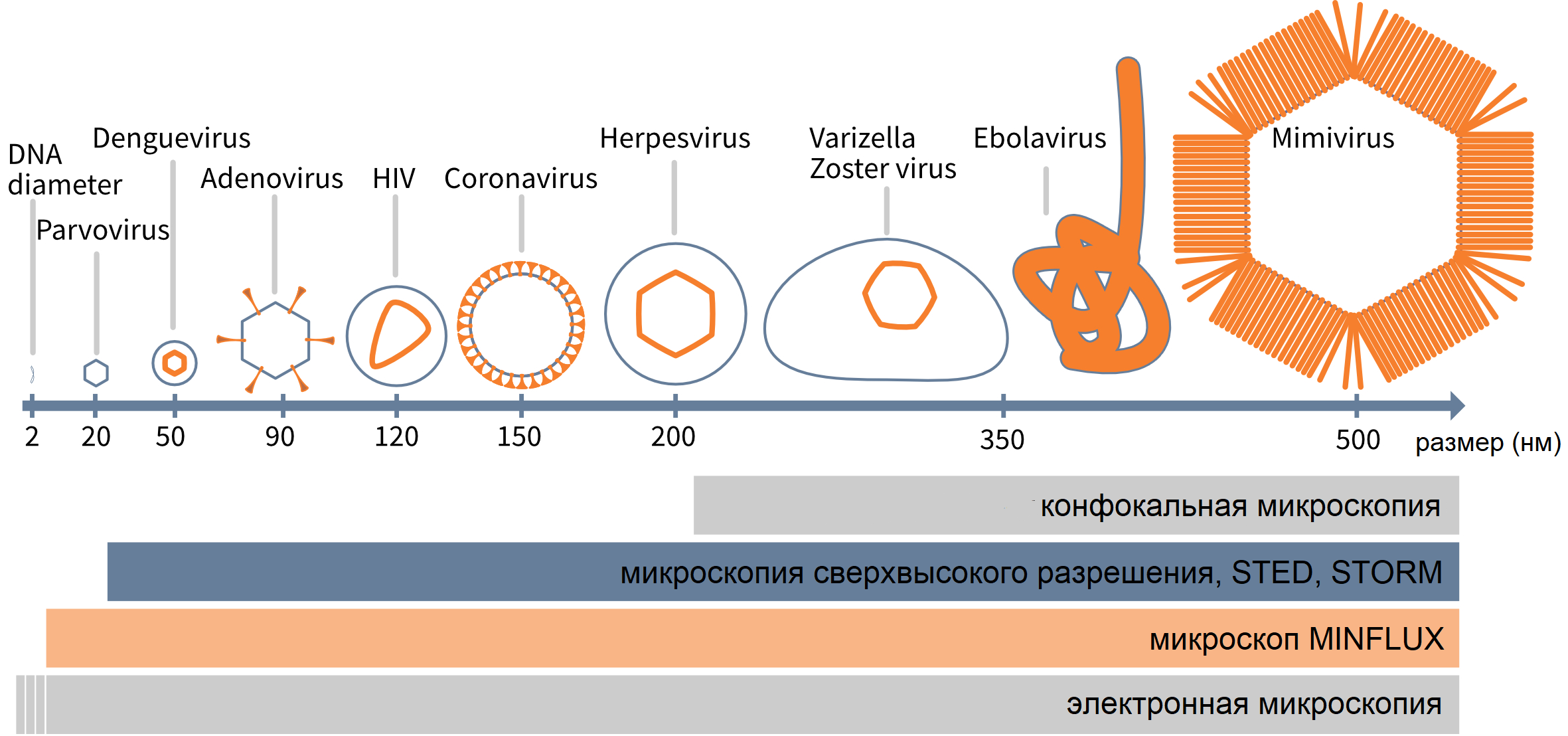
Рис 1: Cравнение различных размеров вирусных частиц с разрешением различных методов визуализации
STED микроскопия для исследования вирусов
Золотым стандартом метода визуализации вирусных частиц была и остается электронная микроскопия (ЭМ). Главным преимуществом метода электронной микроскопии является, несомненно, разрешение в ангстрем-диапазоне, которое превосходит разрешающие возможности всех других доступных методов визуализации. Чрезвычайно высокое разрешение, однако, достигается за счет сильной фиксации образцов с низким контрастом. Кроме того, маркировка и обнаружение специфических белков внутри больших скоплений организмов и клеток является сложной задачей при работе на электронном микроскопе. С другой стороны, методы световой микроскопии, и особенно конфокальная флуоресцентная микроскопия, генерируют высококонтрастные изображения со специфическими метками для интересующих белков. Однако разрешающая способность этих методов ограничена примерно половиной длины волны света (~200 нм). Нобелевские лауреаты по методам микроскопии сверхвысокого разрешения, в частности STED-микроскопии и микроскопии локализации одиночных молекул, преодолевают этот барьер разрешения, используя включение-выключение флуоресцентных красителей. Эти методы улучшают конфокальное разрешение примерно в 10 раз, достигая возможностей разрешения, более близких к тем, которые предлагает электронный микроскоп (см. Рис.1). Кроме того, наноразмерное разрешение STED-микроскопии в сочетании с менее деструктивными методами пробоподготовки и маркировки флуоресценции позволяют изучать структурную информацию нативных (незафиксированных) вирусных частиц в 100 нм диапазоне. Пример того, как STED микроскопия внесла свой вклад в исследование ВИЧ-1, подробно описано ниже.
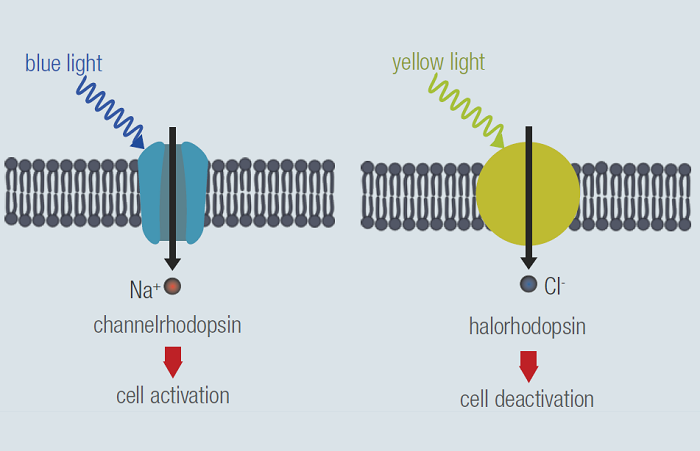
- STED-микроскопия – это сильный метод для наблюдения мельчайших структурных деталей в клетках и вирусах
- Он охватывает весь спектр разрешения, необходимый для изучения вирусов даже в живой среде и во взаимодействии с клетками хозяина
- Метод MINFLUX откроет совершенно новые пути визуализации вирусов
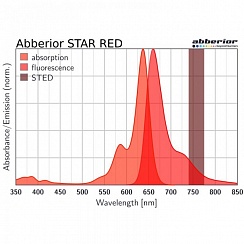
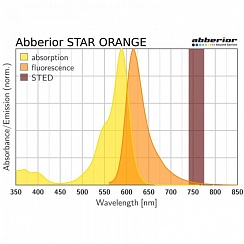
Специфичная для белков маркировка в сочетании с высококонтрастной визуализацией световой микроскопии позволяет колокализационным исследованиям различных белков пролить свет, например, на взаимодействие вируса и хозяина. Однако в классической световой микроскопии понимание положения белка размыто из-за пределов дифракции. Методы микроскопии сверхразрешения преодолевают этот эффект размытия и, таким образом, придают гораздо более высокую достоверность результатам экспериментов по колокализации. STED-микроскопия особенно хорошо подходит для этих исследований, поскольку разрешение может быть улучшено не только в боковом, но и в осевом направлении, что приводит к изотропному разрешению до 60 нм без какой-либо постобработки. Кроме того, если используются два спектрально различных красителя, которые могут быть возбуждены одним и тем же лазерным «пончиком» STED (например, STAR ORANGE и STAR RED, или Alexa594 и ATTO647N), то хроматический сдвиг между этими двумя каналами отсутствует. Поскольку центральный ноль «пончика» STED излучения определяет точку, из которой испускаются фотоны, если два канала разделяют один и тот же «пончик» возбуждения, колокализация внутренне задана. В различных исследованиях использовали STED-микроскопию для визуализации генома вируса простого герпеса внутри инфицированных клеток или для изучения взаимодействия вируса гриппа А с хозяином.
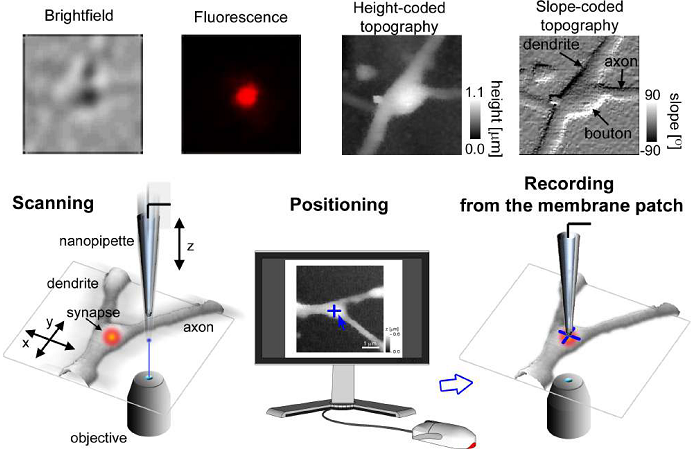
Возможность визуализации живых клеток и отслеживания динамических событий во времени является большим преимуществом флуоресцентной микроскопии, и STED-микроскопия уникально сочетает это преимущество с наноразмерным разрешением. STED-микроскопия живых клеток доказала свою ценность во многих исследованиях. Одной из основных проблем в микроскопии живых клеток STED является отбеливание и фототоксичность. В то время как отбеливание можно преодолеть с помощью фотостабильных красителей или сменных флуорофоров, минимизация фототоксичности менее проста. Тем не менее, при использовании STED-микроскопии часто упускается из виду, что разрешение и мощность лазера взаимозависимы. Из-за зависимости квадратного корня разрешения от мощности STED-лазера высокая мощность этого лазера необходима только для того, чтобы реализовать последние несколько нанометров разрешения. В STED-микроскопии достигаемое разрешение настраивается с помощью мощности STED-лазера, и оно может быть увеличено настолько, насколько это необходимо для ответа на заданный научный вопрос. Кроме того, новые технологии, такие как STED с импульсным лазером в сочетании с адаптивными методами освещения (например, MINFIELD, DyMIN и RESCue), позволяют проводить длительную визуализацию в высоком разрешении с низким уровнем освещенности и, следовательно, с меньшим количеством фототоксических эффектов. Пример визуализации ВИЧ-1 показан на Рис.2. Здесь также важно отметить, что поскольку вирусная частица содержит лишь небольшое количество белков и, следовательно, меток, мягкие адаптивные методы освещения помогают свести к минимуму фотообесцвечивание, что позволяет получить изображение с более высоким разрешением или в течение более длительного времени в живом эксперименте.

Рис. 2: Исследование MINFIELD STED, представленное на вирусе иммунодефицита человека Типа 1 (ВИЧ-1, меченный SNAP-тегом между матрицей и капсидом в белке Gag и окрашенный Силикономродамином). (А) Конфокальные (слева) и полутоновые (справа) изображения с размером поля 160 нм. B) схема незрелой частицы ВИЧ-1 с метками, обозначенными красным цветом. С) примеры визуализации отдельных частиц ВИЧ-1.
Особенно редкие события трудно поддаются визуализации на электронном микрокопе и обычно могут быть обнаружены только с помощью корреляционной визуализации световой микроскопии и электронного микроскопа. Идентификация разреженных событий, таких как клеточная инфекция или связывание вирусных частиц для проникновения в клетку или ядро, является идеальной мишенью для STED-микроскопии. Поскольку каждый STED-микроскоп по своей сути является конфокальным микроскопом (с выключенным STED-лазером), и позволяет сканировать образец в конфокальном режиме с помощью объектива с низким увеличением, чтобы легко идентифицировать редкие события. После обнаружения события можно выбрать интересующую область для наведения на него, а затем включить STED-лазер, чтобы получить изображение со сверхвысоким разрешением. Визуализация капсид-позитивных объектов после ВИЧ-инфекции клеток, близких к ядерной поре, является одним из примеров того, как STED-микроскопия может быть использована для изучения редких событий.
Научные исследования, связанные с визуализацией вирусов, требуют большого диапазона масштабов визуализации – от одной вирусной частицы на покровном стекле до целых инфицированных клеток или даже интактных живых мышей, чтобы, например, наблюдать иммунный ответ в лимфатических узлах. Таким образом, идеальная микроскопия сверхвысокого разрешения должна быть гибкой для выполнения всех задач визуализации. Микроскопы STED надежно отвечают этой потребности и могут быть адаптированы для различных экспериментов по визуализации. Объективы и установочные носители могут быть выбраны по мере необходимости для проведения эксперимента. Адаптивная оптика позволяет получать STED- и конфокальное изображение глубоко внутри образца с помощью деформируемого зеркала для коррекции аберраций, вызванных образцом. Имея под рукой эти инструменты, микроскоп STED способен создавать изображения в разных масштабах и хорошо адаптируется к потребностям экспериментатора.
Обзор исследования ВИЧ-1 с помощью STED микроскопии
Созревание вируса иммунодефицита человека 1 (ВИЧ-1) происходит одновременно с отщеплением от плазматической мембраны его клетки-хозяина. Во время созревания протеаза активна и расщепляет полипротеиновый кляп на его компоненты, что приводит к перестройке вирусных белков. Зрелые частицы ВИЧ проникают в клетки более эффективно. Однако явного изменения структуры или состава поверхностного белка (белка оболочки, Env) не наблюдается. По сравнению с другими вирусными частицами, только несколько белков оболочки включены на поверхность ВИЧ (7-14 белков Env на вирусную частицу). Остается открытым вопрос о том, как внутреннее морфологическое изменение влияет на белок Env на поверхности частиц и каков поверхностный эффект, повышающий эффективность проникновения в новые клетки-хозяева.
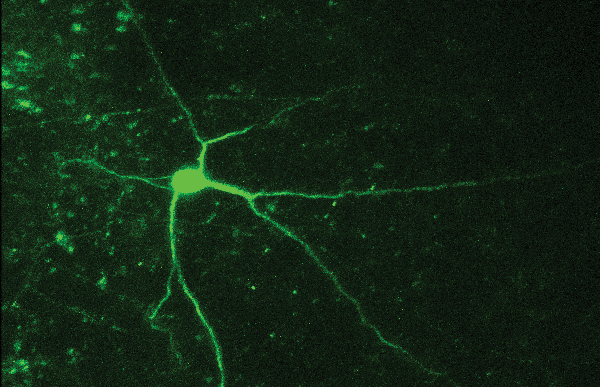
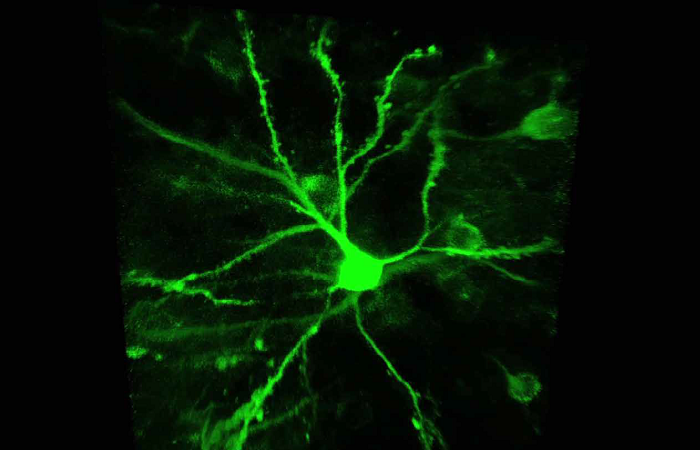
В 2012 году исследовательская группа Hans-Georg Kräusslich ответила на эти вопросы с помощью STED-микроскопии, когда метод был еще в зачаточном состоянии. В сотрудничестве с группой Стефана Хелла они показали, что белки Env на отдельных вирусных частицах образуют кластеры после созревания вируса, и что эта кластеризация индуцируется созреванием через взаимодействие между хвостом Env и внутренними вирусными белками. Поскольку вирусные частицы (диаметр ~120-150 нм) значительно меньше дифракционного предела света, только прямое наблюдение с помощью микроскопии сверхразрешения позволило разрешить эту кластеризацию (см. Рис.3).

Рис. 3: Распределение белка Env (красный / желтый) на отдельных частицах ВИЧ-1 (зеленый). Краситель Vpr.eGFP был использован в качестве маркера для частиц ВИЧ-1. Кластеры Env на поверхности вирусных частиц были помечены Fab-фрагментами, связанными со STAR635P. Только с помощью микроскопии сверхразрешения можно выявить отдельные кластеры Env (сравните среднюю колонку (STED) и правую колонку (конфокальная микроскопия)).
В последующем исследовании, проведенном в Оксфордском университете, исследователи смогли определить подвижность Env-тримеров на одной вирусной частице. Это исследование показало, что липидная оболочка ВИЧ-1 представляет собой среду с низкой подвижностью из-за ее высокого порядка липидов. Стандартным методом определения подвижности изображений является флуоресцентная корреляционная спектроскопия (ФКС). Однако, поскольку вирусные частицы меньше обычного сфокусированного пятна, флуктуации интенсивности, обусловленные движением частиц, могут наблюдаться только при сочетании STED и ФКС, чтобы уменьшить фокальный объем.
Наблюдаемый высокий липидный порядок привел к сотрудничеству между лабораториями в Испании, Франции, Германии и Австралии для изучения липидной среды зарождающихся частиц ВИЧ в клетках с помощью STED- ФКС. Исследование показало, что вокруг места зарождения ВИЧ-1 вирус, по-видимому, генерирует свою собственную липидную среду, что, вероятно, связано с рекрутированием специфических липидов через основной структурный Gag полипротеин.
Таким образом, основной вклад в фундаментальные исследования ВИЧ-1 был внесен с помощью STED-микроскопии. Кроме того, в будущем STED и микроскопия сверхвысокого разрешения в целом будут играть важную роль в исследованиях небольших структур, таких как вирусы.
Заключение и перспективы
В данной статье приводится краткий обзор микроскопии сверхвысокого разрешения с акцентом внимания на микроскопии STED и ее вкладе в визуализацию вирусов и вирусные исследования. Развитие инструментария STED-микроскопии идет быстрыми темпами и, хотя этот метод уже получил широкое распространение в научных исследованиях, мы уверены, что его потенциал будет только увеличиться в будущем. Не следует забывать, что первые изображения на самодельном микроскопе STED были получены лишь менее двух десятилетий назад. С тех пор огромное количество технических разработок и инноваций сделали STED-микроскопию тем, чем она является сегодня: надежным, простым в использовании методом визуализации с супер-разрешением, который может использоваться исследователями так же интуитивно, как конфокальный микроскоп.
Потенциал микроскопии сверхвысокого разрешения простирается далеко за пределы STED. Новая методика MINFLUX предлагает изотропное разрешение до 2 нм – размер одной флуоресцентной молекулы. STED-микроскопия уже смогла изменить то, как мы смотрим на вирусные частицы, поэтому влияние, которое она окажет на научные исследования, нельзя недооценивать. Этот новый уровень разрешения, как ожидается, окажет огромное влияние на вирусологические исследования. Отслеживание MINFLUX может быть выполнено на чрезвычайно высоких скоростях с молекулярной точностью, что позволяет наблюдать перегруппировки внутри одного белка с течением времени или следить за отдельными вирусными частицами в течение длительного времени с беспрецедентной точностью и скоростью.