Вступление
Долгосрочная цель нейробиологии - выяснить, как сложные нейронные цепи связаны с поведением. Появление кальциевой визуализации предоставило исследователям мощный метод измерения активности отдельных клеток с использованием флуоресцентных показателей кальция (1,2) (см. рисунок 1). Кальциевые индикаторы определяют приток кальция путем испускания флуоресцентного сигнала, который используется в качестве косвенного показателя клеточной активности (1,2). Развитие генетически кодированных индикаторов кальция (GECI - genetically encoded calcium indicators), таких как GCaMP, который генерирует излучение в зеленой области спектра, предоставило исследователям инструмент способный ограничить экспрессию для выбора клеточных популяций, позволяя считывать специфические для клетки активности (1,2). С тех пор визуализация кальция стала методом измерения активности нейронов в естественных условиях с высоким пространственным и временным разрешением. Важно отметить, что развитие передовых оптических инструментов (то есть оптоволоконная фотометрия, миниатюрные микроскопы и волоконные эндоскопы) ускорили считывание нейронной активности во время поведения животных с кальциевой визуализацией (3-5).
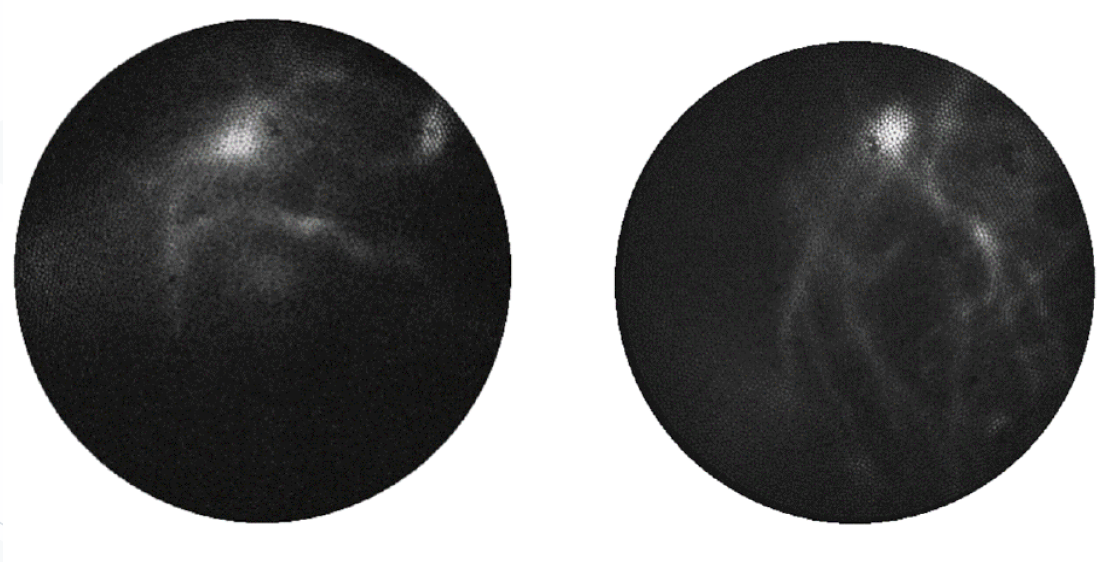
Рисунок 1. Стриатум мыши с GCaMP6. Изображение получено с помощью OASIS Implant Mightex.
Способность визуализировать активность нервной цепи и соотнести это показание с поведением животных является основным преимуществом визуализации кальция. Тем не менее, без возможности манипулировать нейронными цепями исследование может лишь частично определить функциональную связь между нейронными цепями и поведением исследуемого животного. Изобретение оптогенетики стало главной ступенькой к достижению этой цели, так как этот метод позволяет ученым включать или выключать специфические нейронные активности с точностью до миллисекунды, используя свет, чтобы исследовать функцию нейронной цепи в поведении животного. Клетки, экспрессирующие светочувствительные каналы, могут быть стимулированы конкретными длинами волн света, чтобы активировать или ингибировать клеточную активность (6). Оптогенетика произвела революцию в нейробиологии, предоставляя исследователям возможность оптически контролировать нервную активность во время поведенческих событий, чтобы понять их функциональные взаимоотношения.
Интеграция оптогенетики с in vivo визуализацией кальция может помочь охарактеризовать точную связь между нейронными цепями (деятельность и функция) и поведением. Исследования с использованием in vivo визуализации кальция обеспечивают функциональный выход нейронных цепей по отношению к поведению. Используя оптогенетику, извлеченный нейронный код может быть введен для измерения поведенческого выхода. Эти оптические методы обеспечивают высокий пространственный и временной контроль, чтобы понять эти отношения с разрешением на уровне отдельных клеток. Все оптические методы (комплексная кальциевая визуализация и оптогенетика) могут эффективно использоваться как для «чтения», так и для «записи» для управления поведением с обратной связью с помощью передовых оптических инструментов для in vivo визуализации кальция и оптогенетики (4,7,8).
В этой статье сначала детально описываются биологические аспекты интеграции кальциевой визуализации и оптогенетики. Ниже будут приведены и рассмотрены все оптические инструменты, используемые для получения изображений и оптогенетики, а также сравнение этих методов с точки зрения преимуществ и недостатков. Также в этой статье будет обсуждаться, как эти инструменты используют визуализацию кальция и оптогенетику для исследований в области неврологии в естественных условиях и как они могут помочь исследователям понять прямую связь между специфической нейронной активностью, разнообразными функциями мозга и поведением.
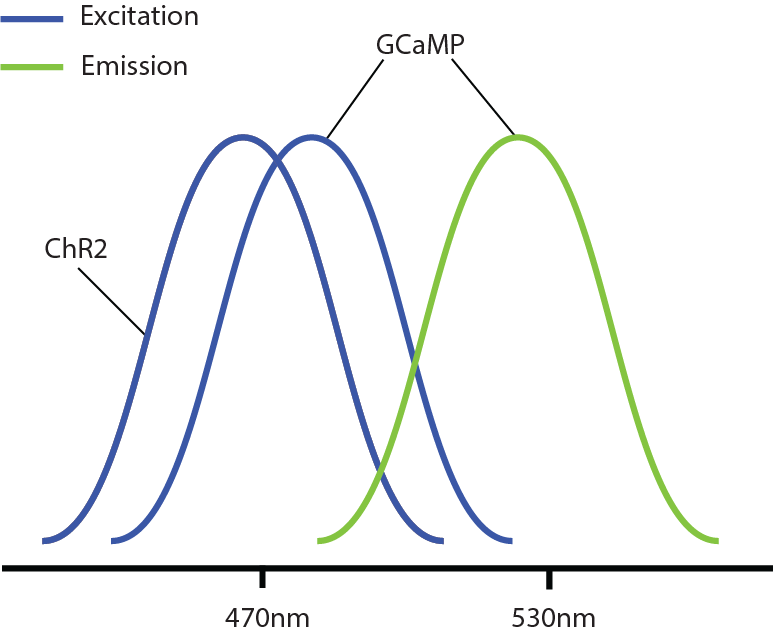
Рисунок 2. Этот график показывает спектры возбуждения GCaMP и ChR2 (значения являются репрезентативными), а также спектр эмиссии GCaMP. Кроме того, на этом рисунке показаны перекрывающиеся спектры возбуждения GCaMP и ChR2. Синий представляет возбуждение и зеленый цвет представляет эмиссию.
Интеграция оптогенетики с визуализацией кальция
GECI ведут себя так же, как флуорофоры (например, GFP), у них есть спектры возбуждения и эмиссии. Тем не менее, флуоресцентный сигнал GECI зависит от внутриклеточной концентрации кальция (то есть излучение флуоресценции усиливается из-за повышенного притока кальция) и отображает динамическое поведение в отличие от статического сигнала от флуорофора (1,2). Напротив, оптогенетические зонды имеют спектры возбуждения для активации их активирующих/ингибирующих свойств (3).
Исследователи обычно предлагают использовать GCaMP для визуализации и каналродопсин (ChR2) для оптогенетики в полностью оптических экспериментах для оптимизации, эффективности и из-за частого использования этих биологических зондов. Тем не менее, GCaMP и ChR2 имеют перекрывающиеся спектры возбуждения (пиковая длина волны ~ 470 нм), что означает, что когда GCaMP и ChR2 экспрессируются в одной ткани, то возбуждение кальциевой визуализации может потенциально стимулировать также оптогенетический зонд (см. рисунок 2). Следовательно, визуализация GCaMP и оптогенетическая стимуляция ChR2 не может быть выполнена одновременно из-за оптических перекрестных помех, и нет возможности определить, чем вызваны измеренные изменения в GCaMP сигнале, вследствие естественных изменений в активности или оптогенетических изменений.
Оптические перекрестные помехи могут быть уменьшены путем селективного выбора индикатора визуализации и оптогенетического зонда, используемые для полностью оптических экспериментов на основе их спектров возбуждения. Примеры таких комбинаций с наименьшими оптическими перекрестными помехами - синее возбуждение/зеленое излучение (например, GCaMP) и оптогенетика со смещением в красную область спектра (например, Chrimson, Jaws) или зеленое возбуждение / красная эмиссионная визуализация (например, RCaMP) и оптогенетика со смещением в синюю область спектра (например, ChR2, GtAChR). Хотя и существует некоторое совпадение между спектрами возбуждения этих зондов вероятность того, что перекрестные помехи будут снижены, предотвращает косвенную активацию Вашей оптогенетической конструкции во время получения изображения. Дальнейшая оптимизация визуализации и оптогенетических зондов (например, чувствительность, спектры возбуждения) поможет предотвратить оптические перекрестные помехи.
Оптические инструменты для интегрированных in vivo кальциевой визуализации и оптогенетики
Совсем недавно исследователи пытались интегрировать оптогенетику в их эксперименты по визуализации кальция со свободно движущимся исследуемым животным, чтобы отметить связь между нейронными цепями и поведением. Для выполнения этих передовых экспериментов необходимы специализированные инструменты для чтения и записи нейронных кодов в животном со свободным поведением. Здесь мы рассмотрим три инструмента в настоящее время используемых для проведения таких экспериментов: (1) оптоволоконная фотометрия, (2) миниатюрные микроскопы и (3) оптические фиброскопы.
Оптоволоконная фотометрия
Оптоволоконная фотометрия - это полностью оптический метод для одновременной регистрации кальциевого сигнала и оптогенетики в мозге свободно перемещающихся животных. Этому методу не хватает пространственного разрешения, которое позволяет «видеть» или «контролировать» отдельные нейроны, но он способен регистрировать сигнал популяции (см. рисунок 3а). Имплантированная оптическая канюля в сочетании с оптическим волокном посылает свет в мозг исследуемого животного и одновременно извлекает кальциевые сигналы для передачи на внешний фотоприемник или камеру для обеспечения как стимулирующих, так и регистрирующих сигнал функций (4,9).
Для регистрации кальциевого сигнала система для оптоволоконной фотометрии регистрирует среднюю интенсивность флуоресценции, которая изменяется от нейронной активности популяции в выбранной области мозга свободно перемещающегося животного (4,9). Таким образом, исследователи могут зарегистрировать активность генетически определенной популяции нейронов, и эта особенность делает оптоволоконную фотометрию простым низкоуровневым методом получения кальциевого сигнала. Кроме того, метод оптогенетики может быть легко интегрирован в установку оптоволоконной фотометрии, чтобы добиться одновременного обнаружения кальциевого сигнала и опотогенетики (см. рисунок 4). Используя несколько волокон в комбинации с камерой, а не фотодетектором, визуализация кальция и оптогенетика могут быть выполнены в нескольких областях мозга, чтобы изучить участие проекций или различных областей мозга.
Ограничением оптоволоконной фотометрии является отсутствие пространственного разрешения, ограничивающее фоторегистрацию изменений в активности популяции в пределах выбранной области, и этот метод также ограничен широкопольной оптогенетической стимуляцией и не имеет возможности фокусироваться на отдельных нейронах (4,9,10). Следовательно, метод оптоволоконной фотометрии не позволяет разделять клеточную активность в выбранных нейронах. Тем не менее, этот метод отличают отсутствие результатов пространственного разрешения в небольших файлах данных, быстрое получение и легкая интерпретация данных, в отличие от других современных инструментов кальциевой визуализации. Когда дело доходит до экспериментов в множестве исследуемых областей мозга применение широкопольных методов стимуляции не позволяет исследователям фокусировать оптогенетическую стимуляцию в определенных областях интереса.
Оптоволоконная фотометрия является полезным инструментом, который может дать исследователям лучшее понимание устройства мозга на низком уровне. Упрощенная конструкция и вывод данных с помощью этого метода обеспечивают одновременную визуализацию кальция и оптогенетическую стимуляцию нейронной активности.
Миниатюрный микроскоп
Конструкция миниатюрного микроскопа дает возможность получить изображение активности популяций нейронов с одноклеточным разрешением у животных со свободным поведением (см. рис. 3б). Этот инструмент объединяет в себе все необходимые технологии однофотонного микроскопа, который может быть установлен на голове исследуемого грызуна для in vivo визуализации кальция (3). Соединительная муфта миниатюрного микроскопа с имплантированной в мозг GRIN линзой позволяет этому устройству передавать свет и отображать глубокие области мозга (3).
Миниатюрный микроскоп обеспечивает широкое поле обзора для визуализации кальция, которое определяется размером имплантируемой GRIN линзы и выбор линзы будет зависеть от исследуемой области интереса (11). Кроме того, оптогенетика может быть встроена в миниатюрный микроскоп для выполнения широкопольной оптогенетики в сочетании с кальциевой визуализацией (см. рисунок 4). Тем не менее, для этого требуется специальный минископ, обладающий такой возможностью, т.к. компоненты данного минископа обычно фиксируются на голове животного и не являются модульными (12,13).
Миниатюрная конструкция микроскопа устанавливаемого на голову, который позволяет животному свободно перемещаться, накладывает ограничения на интегрированные в него компоненты. Это ограничивает оптогенетические возможности для уровня населенности без оптогенетики с клеточным разрешением. Кроме того, они включают в себя камеру начального уровня с низкой чувствительностью и высоким уровнем шума и количество длин волн, которые могут использоваться в минископе для освещения, в настоящее время ограничены одной или двумя длинами волн (10-12). Таким образом, возможности этой системы и гибкость для будущих обновлений в настоящее время ограничена. Миниатюрные микроскопы расширили наше понимание нервной деятельности, связанной с памятью, голодом и другими специализированными функциями (12-15). Эта система может обеспечить дальнейшее понимание деятельности больших популяций нейронов для кальциевой визуализации свободно перемещающемся животном.
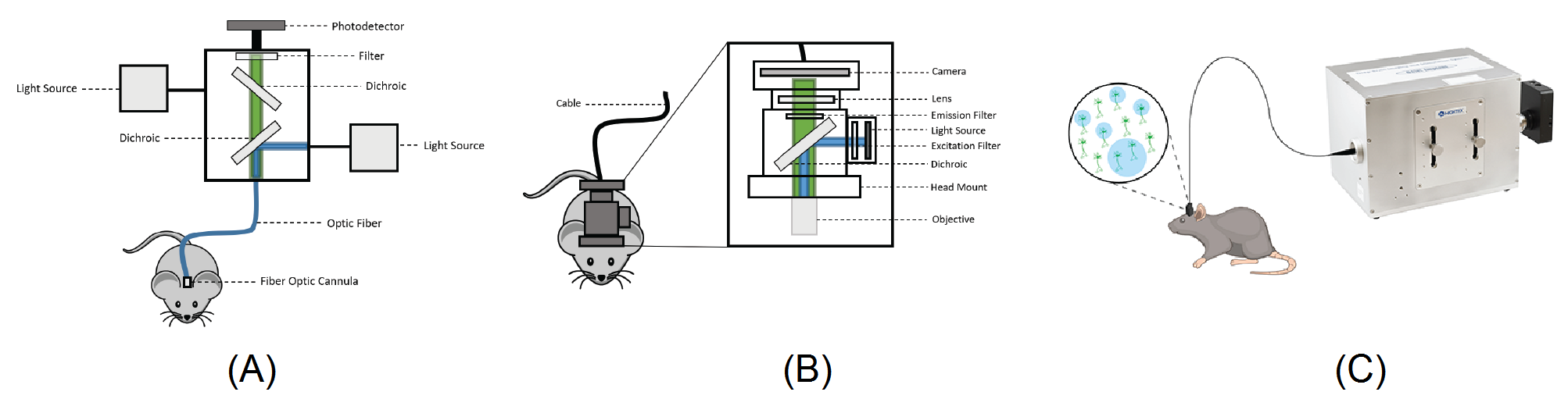
Рисунок 3. (A) Схема оптоволоконной фотометрической системы. (B) Схема миниатюрной микроскопической системы. (C) Схема оптического эндоскопа.
Оптический эндоскоп
Оптический эндоскоп, такой как OASIS implant компании Mightex - это полностью оптическая система, которая позволяет одновременно осуществлять визуализацию и манипуляцию нейронной активности с клеточным разрешением в глубокой области мозга, коре или нескольких областях мозга животного со свободным поведением (см. рис. 3в). Съемное оптическое волокно в сочетании с GRIN линзой или микролинзой имплантированной в мозг обеспечивает как клеточное разрешение изображения и оптогенетические возможности на клеточном уровне.
Отдельные нейроны могут быть различимы при кальциевой визуализации в животном со свободным поведением при использовании оптического эндоскопа. Как и в миниатюрном микроскопе, поле зрения оптического эндоскопа определяется размером имплантированной GRIN линзы. К тому же, оптогенетика легко интегрируется в эксперименты кальциевой визуализации с оптическим эндоскопом (5). Важно отметить, что оптогенетика может быть выполнена с клеточным разрешением для стимуляции отдельных нейронов в свободно перемещающемся животном, что до сих пор не представлялось возможным с помощью методов оптоволоконной фотометрии или при использовании миниатюрного микроскопа (см. рисунок 4). Благодаря использованию волокон с раздельным получением изображения исследователи могут выполнить кальциевую визуализацию и оптогенетику клеточного разрешения в определенных областях интереса в одном или одновременно в нескольких свободно перемещающихся животных с помощью оптического эндоскопа.
Важное преимущество оптического эндоскопа заключается в уникальной гибкой конструкции, которая является масштабируемой и реконфигурируемой, что делает ее основной платформой для визуализации и стимуляции, которая может быть адаптирована для различных применений в отличие от многих других систем. Два оптических пути освещения позволяют исследователям прикрепить несколько широкопольных и/или стимулирующих источников света с разными длинами волн и использовать различные оптические фильтры (например, дихроичные и т. д.), подходящие для различных изображений и/или потребности в освещении. К тому же, эта система совместима с научными камерами высокой чувствительности для получения наилучшего качества изображения (например, с лучшим соотношением сигнал/шум и более высокой линейностью) для анализа данных.
Обладая возможностью одновременной кальциевой визуализации с клеточным разрешением и стимуляцией оптогенетики на клеточном уровне, оптический эндоскоп представляет собой идеальный инструмент способный помочь исследователям понять, как одноклеточные взаимодействия участвуют в процессах продвинутых функций мозга, которые невозможно идентифицировать другими современными технологиями.
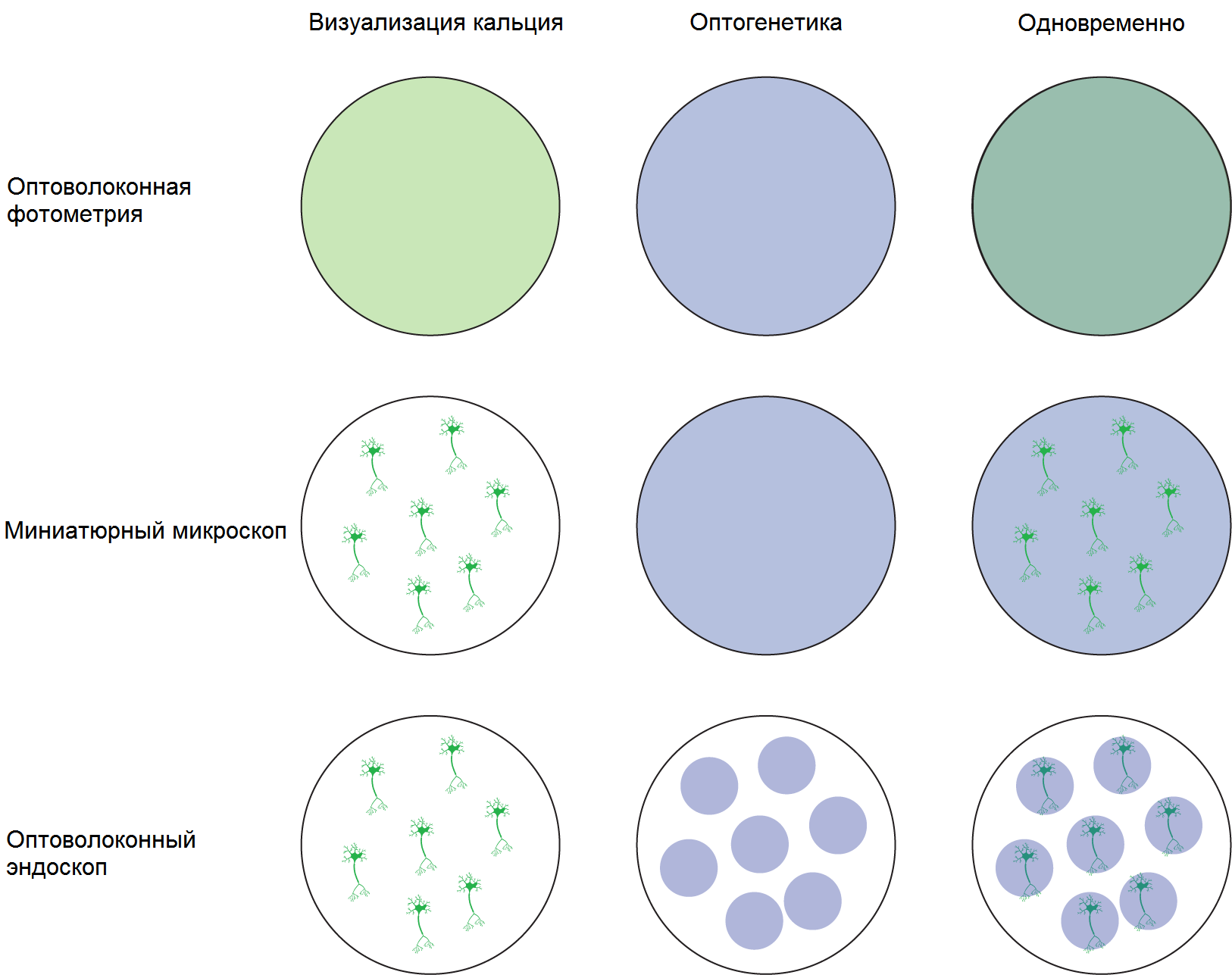
Рисунок 4. На этом рисунке представлен обзор возможностей оптических инструментов для кальциевой визуализации, оптогенетики, одновременной оптогенетики и кальциевой визуализации. Волоконная фотометрия способна обнаруживать кальций на уровне популяции нейронов и выполнить оптогенетику без клеточного разрешения. Миниатюрные микроскопы способны визуализировать кальций с клеточным разрешением, но могут выполнить оптогенетику без клеточного разрешения. Наконец, оптический эндоскоп обеспечивает одновременную визуализацию кальция и оптогенетику с разрешением на уровне клетки.
Полностью оптическая визуализация и оптогенетика
Инструменты для полностью оптической визуализации и оптогенетики могут предоставить исследователям новые возможности в области неврологии. Во-первых, интеграция оптогенетики с визуализацией позволяет исследователям манипулировать проекциями от других областей мозга или локальными входами от разных типов клеток в отношении локально отображаемых клеток для изучения их связи с поведением (12,13). Во-вторых, визуализация кальция у свободно перемещающихся животных позволяет исследователям сформировать функциональный признак, который относится к поведению (например, эти клетки отвечают за нажатие животным на рычаг). Декодирование данных изображения позволит исследователям оптически ввести этот сигнал обратно в нервную систему животного с помощью оптогенетики, чтобы помочь определить функциональные отношения между поведением и мозговыми контурами (7,8). Наконец, одновременная визуализация и оптогенетика имеют потенциал для управления поведением животного в режиме реального времени для контроля активности с обратной связью, чтобы понять прямую связь между деятельностью и поведением (7,8). Все три описанных в данной статье инструмента имеют эти возможности; тем не менее, оптический эндоскоп является единственным прибором для одновременной визуализации с клеточным разрешением и оптогенетики в животном со свободным поведением, чтобы понять функциональные взаимоотношения на клеточном уровне. Вот некоторые из возможных применений, в которых по мере продвижения исследований, эти инструменты могут быть использованы для расширения функциональных возможностей.
Заключение
В заключение стоит отметить, что в настоящее время доступны все оптические технологии интеграции in vivo оптогенетики с кальциевой визуализацией в животных со свободным поведением и каждая из них имеет свои сильные и слабые стороны в зависимости от целевых применений как показано на рисунке 4. Оптоволоконная фотометрия может обнаружить кальциевый сигнал и выполнить оптогенетику на уровне популяции нейронов у свободно движущихся животных с быстрым и простым выводом данных, но этому методу не хватает способности видеть и стимулировать отдельные нейроны. Миниатюрный микроскоп может дать возможности однофотонной микроскопии с клеточным разрешением в мозгу свободно ведущих себя животных, но он может предложить только возможности оптогенетики на уровне населенности и не может фокусироваться на отдельных нейронах. Оптический эндоскоп является единственным инструментом, который одновременно обеспечивает клеточное разрешение оптогенетики и кальциевой визуализации у свободно перемещающихся животных. Эти передовые полностью оптические инструменты помогут исследователям понять прямую связь между специфической нейронной активностью и сенсорными, поведенческими, когнитивными и/или кортикальными события с временными отметками с высоким временным и пространственным разрешением.
Литература
1. Broussard GJ, Liang R, & Tian L (2014). Monitoring activity in neural circuits with genetically encoded indicators. Frontiers in Molecular Neuroscience, 7, 1-17.
2. Lin MZ & Schnitzer MJ (2016). Genetically encoded indicators of neuronal activity. Nature Neuroscience, 19, 1142-1153.
3. Ghosh KK et al. (2011). Miniaturized integration of a fluorescence microscope. Nature Methods, 8, 871-878.
4. Kim CK et al. (2016). Simultaneous fast measurement of circuit dynamics at multiple sites across the mammalian brain. Nature Methods, 13, 325-328.
5. Szabo et al. (2014). Spatially selective holographic photoactivation and funcational fluorescence imaging in freely behaving mice with a fiberscope. Neuron, 84, 1157-1169.
6. Yizhar O et al. (2011). Optogenetics in neural systems. Neuron, 71, 9-34.
7. Emiliani V, Cohen AE, Deisseroth, & Hausser M (2015). All-optical interrogation of neural circuits. Journal of Neuroscience, 35, 13917-13926.
8. Grosenick L, Marshel JH, & Deisseroth K (2015). Closed-loop and activity-guided optogenetic control. Neuron, 86, 106-139.
9. Gundaydin LA et al. (2014). Natural neural projection dynamics underlying social behaviour. Neuron, 157, 1535-1551.
10. Resendez SL & Stuber GD (2015). In vivo calcium imaging to illuminate neurocircuit activity dynamics underlying naturalistic behaviour. Neuropsychopharmacology, 40, 238-256.
11. Resendez et al. (2016). Visualization of cortical, subcortical and deep brain neural circuit dynamics during naturalistic mammalian behavior with head-mounted microscope and chronically implanted lenses. Nature Protocols, 11, 566-597.
12. Stamatakis et al. (2018). Simultaneous optogenetics and cellular resolution calcium imaging during active behavior using a miniaturized microscope. Frontier in Neuroscience.
13. Owen SF et al. (2018). Fast-spiking interneurons supply feedforward control of bursting, calcium, and plasticity for efficent learning. Cell, 172, 683-695.
14. Betley JN et al. (2014). Neurons for hunger and thirst transmit a negative-valence teaching signal. Nature, 521, 180-185.
15. Pinto L & Dan Y (2015). Cell-type specific activity in prefrontal cortex during goal-directed behaviour. Neuron, 87, 437-450.