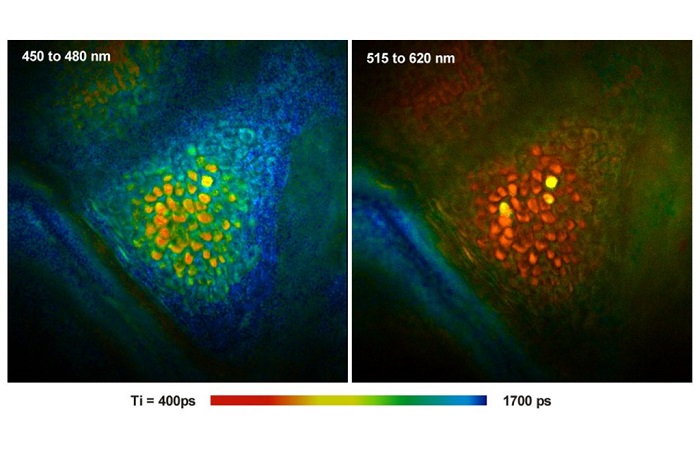
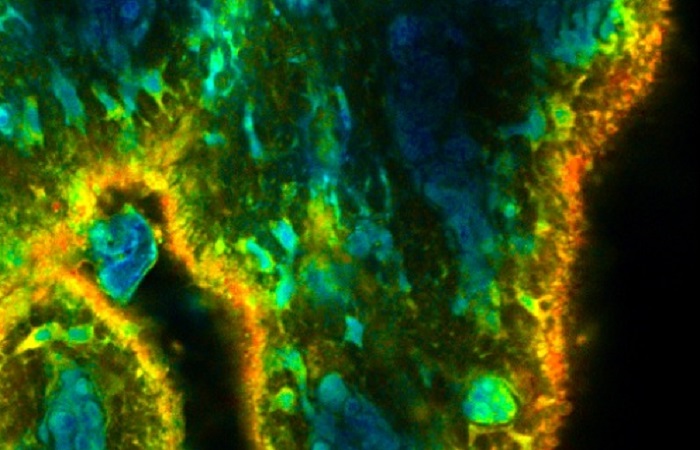
Микроскопия с принудительным подавлением спонтанного излучения (STED - Stimulated-Emission Depletion) использует нелинейность стимулированного излучения для получения оптического сверхразрешения (Hell & Wichmann, 1994). Флуоресценция, возбуждаемая лазерным лучом в сканирующем микроскопе, истощается за счет стимулированного излучения, индуцированного вторым (STED) лазерным лучом. Волновым фронтом пучка STED управляют для получения дифракционной картины, которая имеет либо форму бублика, лежащего в плоскости x-y, либо форму гантели, ориентированную вдоль оси z. Флуоресценция остается не истощенной в центральной части луча в виде пончика или гантели. Поскольку вынужденное излучение сильно нелинейно, неиспользованный объем может быть значительно меньше, чем функция рассеяния точки пучка возбуждения. Сканируя оба луча вместе, получают изображения с оптическим сверхвысоким разрешением.
Поскольку метод STED использует процедуру сканирования и импульсное возбуждение, комбинация с методом FLIM не представляет большой проблемы. Тот факт, что ранняя часть функции распада искажена неполным истощением флуоресценции, можно объяснить, исключив эту часть из анализа времени жизни.
Тем не менее, публикации о молекулярных FLIM-приложениях в STED микроскопии редки. Время жизни флуоресценции в основном используется в качестве параметра дискриминации для различных флуорофоров. Причина, вероятно, в том, что метод STED традиционно использует флуорофоры с максимальной квантовой эффективностью и высокой фотостабильностью. Эти флуорофоры имеют жесткую молекулярную структуру и, следовательно, не проявляют заметных изменений времени жизни в зависимости от молекулярной среды. Потенциальной проблемой в молекулярных применениях являются также дополнительные поглотители в клетках. Эти поглотители могут быть поражены подавляющим лазером. Благодаря высокой мощности они быстро фотообесцвечиваются, что напрямую ухудшает жизнеспособность клеток, либо, по крайней мере, вызывает окислительный стресс. Примерами являются изображения FRET, где лазер STED разрушает акцептор, или NAD(P)H FLIM, где он разрушает FAD. Тем не менее, могут быть полезны приложения, если только STED FLIM будет использоваться с флуорофорами средней квантовой эффективности.
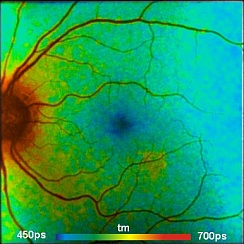
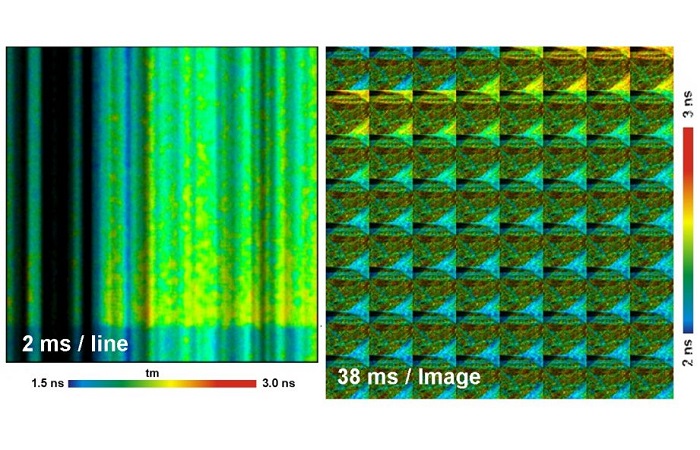
Изображение STED FLIM, записанное модулями счета фотонов SPС-150 с микроскопом Abberior STED (Abberior Instruments, Геттинген, Германия) показано на рисунке ниже.
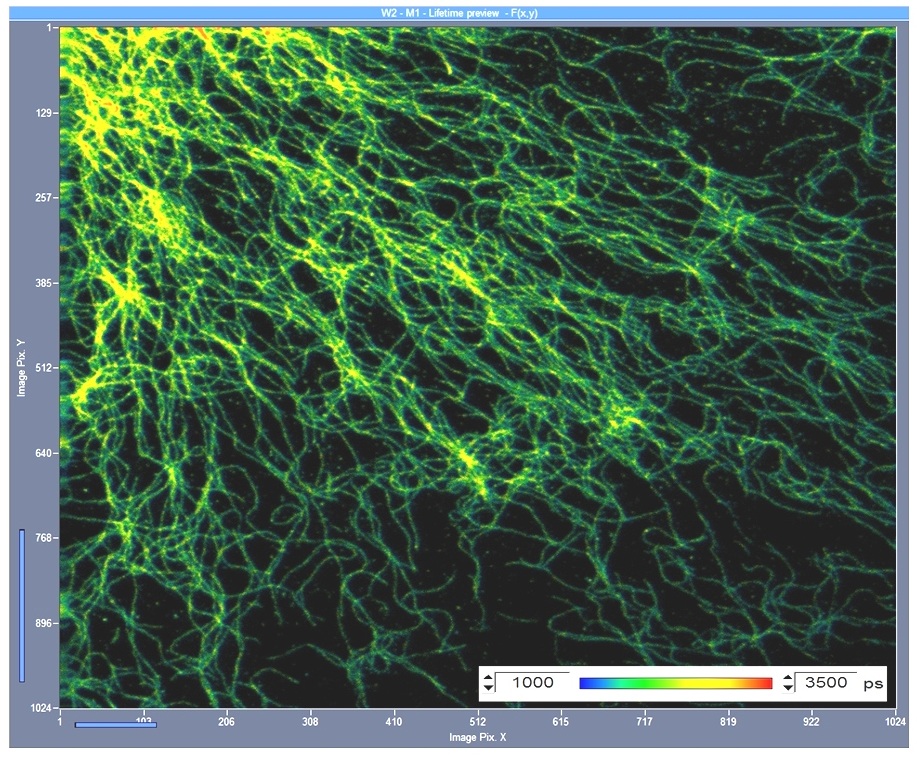
Рис. 1. Микротрубочки в клетке с разрешением 25 нм. Изображение STED FLIM, записанное с помощью микроскопа Abberior STED и FLIM системы SPC‑150 Becker&Hickl. Изображение, созданное с помощью онлайн-функции SPCM. Формат FLIM 1024x1024 пикселей, 256 временных каналов.
Распад флуоресценции, извлеченный из данных, показанных выше, показан на следующем рисунке. Форма распада типична для метода STED. Существует начальный пик не истощенной флуоресценции от всего эйри диска лазера возбуждения, за которым следует функция затухания флуоресценции от молекул в «отверстии» диска истощения. Правильные параметры затухания флуоресценции получают путем подгонки только той части, где истощение завершено. Кроме того, контраст и разрешение можно улучшить, используя только флуоресценцию из истощенной части функции затухания. И то, и другое может быть достигнуто с помощью стандартных функций программного обеспечения для анализа SPCImage FLIM.
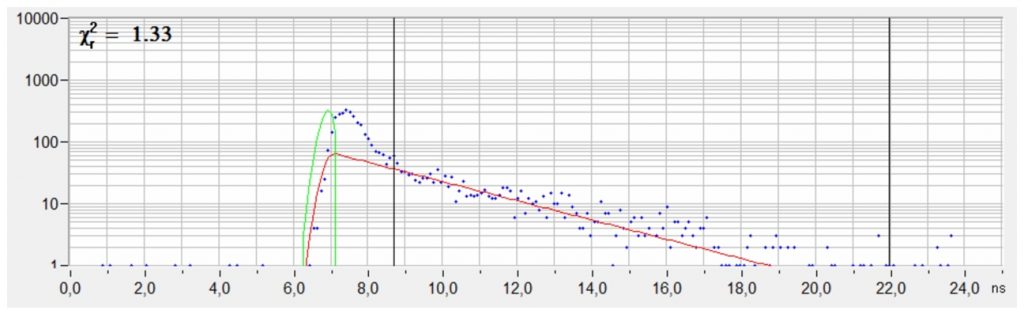
Рис. 2. Кривая затухания от выбранного пятна изображения STED FLIM. Интенсивность флуоресценции и время затухания флуоресценции были получены из временного интервала после пика не истощенной флуоресценции.