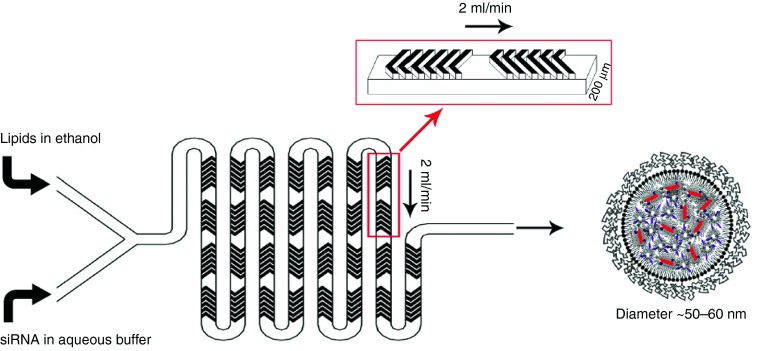
Рибонуклеиновая кислота (РНК) является важной полимерной молекулой для регуляции и экспрессии генов. РНК-интерференция (РНКи) - это метод, при котором происходит подавление экспрессии генов с помощью специфичной для последовательности малой интерферирующей РНК (миРНК, siRNA). На основе нуклеотидных последовательностей, соответствующих мРНК, миРНК блокируют продуцирование специфических белков [1-3]. Для доставки миРНК для терапевтических целей липидные наночастицы (LNP) являются наиболее часто используемой системой для приложений in vivo, таких как противоопухолевые средства или лечение полинейропатий [4-5].
Вакцины BNT162b2 компании BioNTech / Pfizer и Moderna mRNA-1273 также используют липидные наночастицы в качестве носителей для доставки мРНК в цитоплазму клеток-хозяев, что приводит к выработке антител, нейтрализующих COVID [5]. Таким образом, синтез липидных наночастиц сыграл решающую роль в разработке вакцин против COVID-19 и других наномедицинских препаратов и считается очень многообещающим для разработки новых систем доставки лекарств [6].
Липидные наночастицы могут использоваться для других целей, например, для использования твердых липидных наночастиц (SLN) в качестве систем доставки косметики [7].
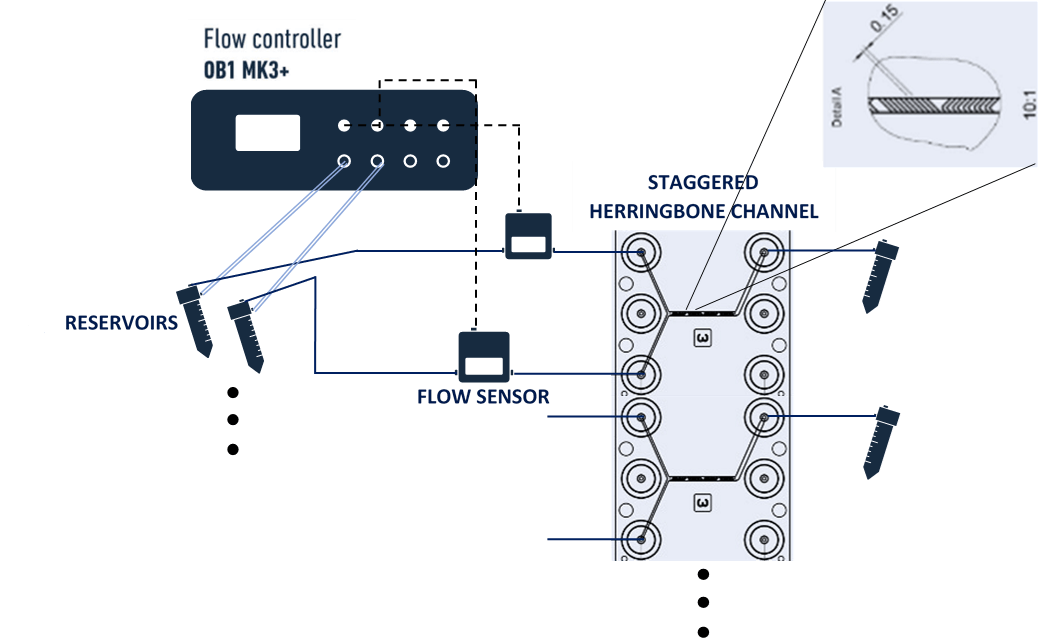
Набор для синтеза липидных наночастиц включает микросмесители с ребристой формой каналов, которые создают хаотические потоки. Они являются наиболее часто используемыми микрофлюидными чипами для синтеза LNP [8]. Структура генерирует хаотическую адвекцию, которая способна вызывать быстрое перемешивание при числах Рейнольдса меньше 1 [9], что обеспечивает лучшую эффективность инкапсуляции, чем объемные методы [10].
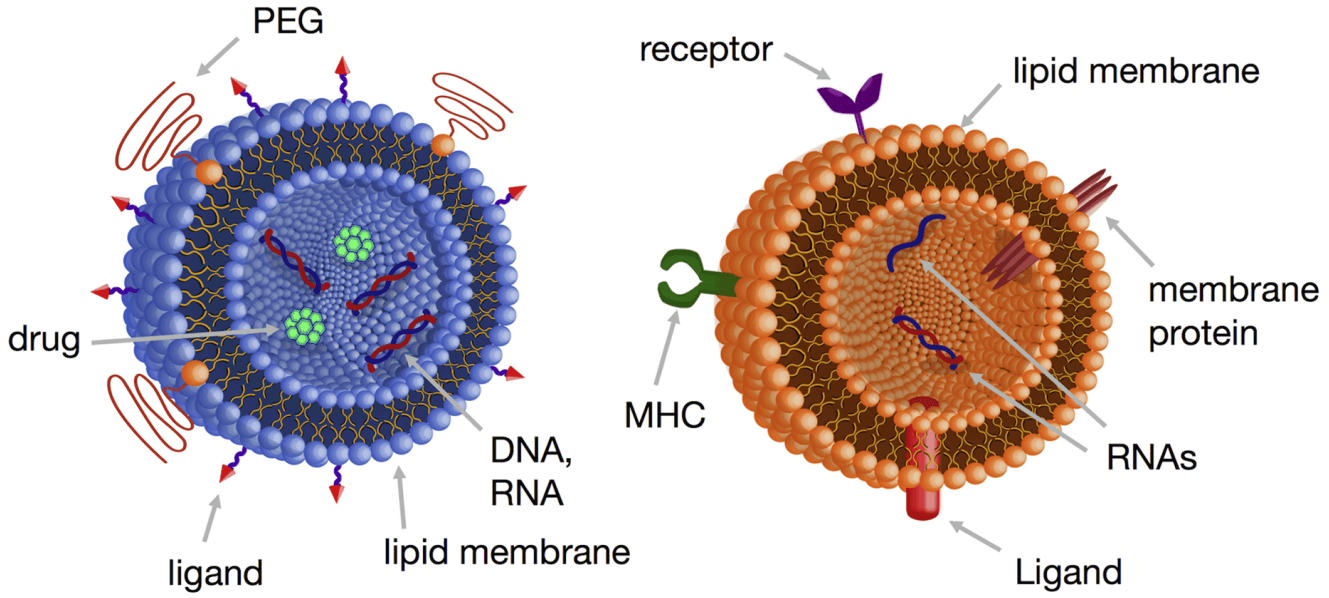
Липидные наночастицы (LNP), состоящие из фосфолипидов, нацеленных лигандов, пегилированных липидов, лекарств и нуклеиновых кислот, а также внеклеточная везикула (EV), содержащая фосфолипиды, рецепторы, белки, нуклеиновые кислоты, молекулы MHC (главного комплекса гистосовместимости) и лиганды [8] .
- Whitehead, K., Langer, R. & Anderson, D. Knocking down barriers: advances in siRNA delivery. Nat Rev Drug Discov 8, 129–138 (2009).
- Belliveau N., Huft J., Lin P., Chen S., Leung A., Leaver T., Wild A., Lee J., Taylor R., Tam Y., Hansen C., Cullis P., Microfluidic Synthesis of Highly Potent Limit-size Lipid Nanoparticles for In Vivo Delivery of siRNA, Molecular Therapy - Nucleic Acids, 1, 2012, e37, 2162-2531
- Allen, Theresa M., and Pieter R. Cullis. "Drug delivery systems: entering the mainstream." Science 303.5665 (2004), 1818-1822.
- Sasayama Y., Hasegawa M., Taguchi E., Kubota K., Kuboyama T., Naoi T., Yabuuchi H., Shimai N., Asano M., Tokunaga A., Ishii T., Enokizono J., 2019, In vivo activation of PEGylated long circulating lipid nanoparticle to achieve efficient siRNA delivery and target gene knock down in solid tumors. Journal of Controlled Release
- Let’s talk about lipid nanoparticles. Nat Rev Mater 6, 99 (2021).
- Thi, T.T.H.; Suys, E.J.A.; Lee, J.S.; Nguyen, D.H.; Park, K.D.; Truong, N.P. Lipid-Based Nanoparticles in the Clinic and Clinical Trials: From Cancer Nanomedicine to COVID-19 Vaccines. Vaccines 2021, 9, 359
- Sylvia A Wissing; Rainer H Müller (2003). Cosmetic applications for solid lipid nanoparticles (SLN), 254(1), 65–68.
- Maeki M., Kimura N., Sato Y., Harashima H., Tokeshi M., 2018, Advances in microfluidics for lipid nanoparticles and extracellular vesicles and applications in drug delivery systems. Advanced Drug Delivery Reviews
- N-T. Nguyen, Z. Wu, Micromixers-a review, J. Micromech. Microeng. 15, 2005, R1-R16.
- Leung A., Hafez I., Baoukina S., Belliveau S., Zhigaltsev I., Afshinmanesh E., Tieleman P., Hansen C., Hope M., and Cullis P., The Journal of Physical Chemistry C 2012 116 (34), 18440-18450