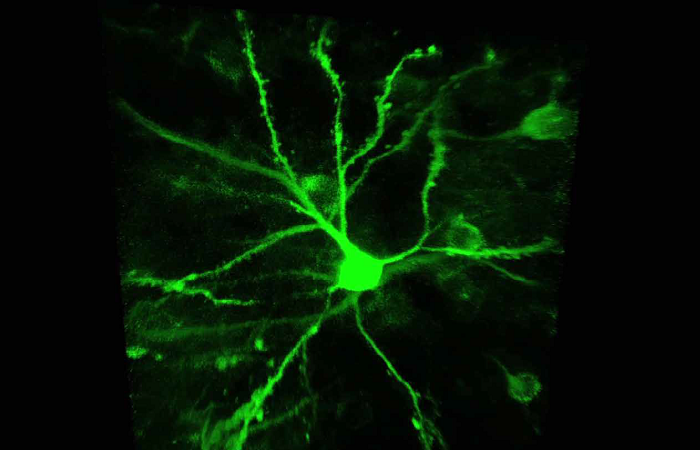
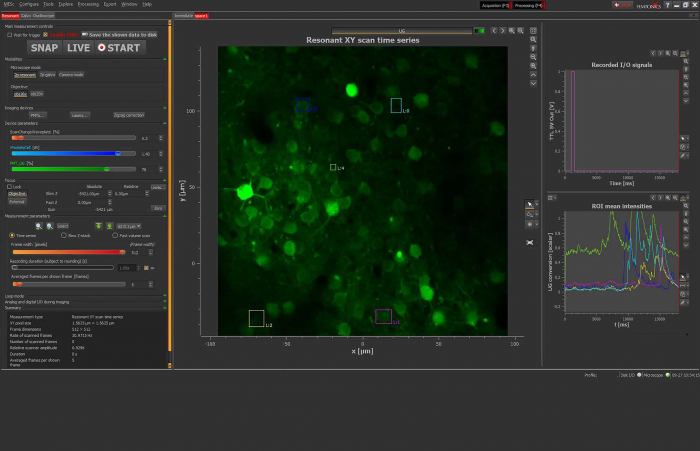
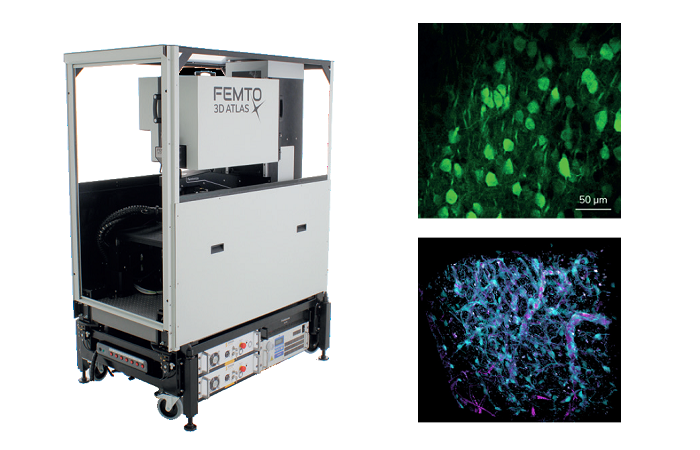
Визуализация одиночных молекул для нейробиологии
Человеческий мозг - одна из самых сложных систем в биологии. Обладая 100 триллионами соединений, нейронная сеть контролирует двигательные реакции и сенсорную информацию, которые определяют нашу память, идентичность, сознание и творческие способности. Понимание того, как мозг функционирует на уровне одной молекулы, является ключом к пониманию основ нейродегенеративных расстройств, включая болезнь Альцгеймера и Паркинсона. Механизмы, лежащие в основе дегенерации мозга, остаются в значительной степени нерешенными - текущие усилия сосредоточены на понимании его молекулярных свойств, чтобы улучшить раннюю диагностику и разработать более эффективные лекарства.
Часть 1
Изучение нейронных связей
Функции мозга управляются через нейронные связи между дендритными шипами и окончаниями аксонов, известными как синапсы. Синапсы работают сложным и согласованным образом, чтобы поддерживать функцию мозга и адаптироваться/реагировать на раздражители.
|
Проблемы в понимании синапсов Небольшой размер синапсов, менее 200 нм, может затруднить изучение молекулярных механизмов, регулирующих нейротрансмиссию. Каждый синапс состоит из более чем 200 белков и синаптической щели, через которую осуществляется коммуникация между терминалами клетки, размер которой может составлять всего 20-40 нм (рис. 1). Понимание важнейших механизмов, определяющих нейронные связи в состоянии здоровья и болезни, ограничено множеством факторов. Во-первых, культивирование клеточных линий для определенных типов клеток головного мозга может быть трудным для получения и поддержания in vitro, что затрудняет поиск действительно прогностических нейронных моделей. В настоящее время в наиболее доступных исследованиях визуализации сверхвысокого разрешения используются первичные культуры кортикальных клеток и клеток гиппокампа мышей или крыс. Тем не менее, эти модели можно рассматривать как искусственные среды с малой сложностью архитектуры мозга. Привлекательной альтернативой для нейробиологов является использование нейронов, дифференцированных от ИПСК (индуцированных плюрипотентных стволовых клеток, полученных непосредственно из взрослых клеток), что позволяет проводить исследования на линиях клеток человека. Однако отсутствие моделей заболеваний, необходимых для ИСПК, ограничивает исследования с использованием этого подхода. Еще одно ограничение нейровизуализации - доступность инструментов маркировки, так как доступные антитела нацелены на наиболее распространенные и наиболее изученные белки, в то время как другие участники остаются неизученными, что затрудняет подробный анализ архитектуры нейронных синапсов. |
Рисунок 1. Схематическое изображение синапса человеческого мозга. Пресинаптические молекулы помечены фиолетовым и зеленым цветом, а постсинаптическая плотность (PSD) показана красными и оранжевыми молекулами. |
Одномолекулярная нейровизуализация
|
Поскольку размер синапсов меньше 200 нм их сложные молекулярные детали «невидимы» для обычных методов световой микроскопии ограниченной дифракцией. Понимание молекулярных признаков пластичности мозга с чувствительностью к одиночным молекулам влечет за собой характеристику архитектуры синапсов нейронов и изучение динамики синаптических белков, включая молекулярные взаимодействия и распределения нейромедиаторов, нуклеиновых кислот и других биомолекул. Визуализация одиночных молекул - надежный инструмент для ответа на фундаментальные вопросы о функциях и дисфункциях мозга, особенно в сочетании с исследованиями сложных взаимодействий в нейрональной экосистеме. В представленном примере синапсы нейронов были визуализированы в трехцветной визуализации методом dSTORM микроскопии с использованием двух пресинаптических белков; Фагот (синаптическая активная зона, пурпурный) и VGluT1 (синаптические пузырьки, зеленый) и постсинаптический белок Homer1 (постсинаптическая плотность, оранжевый). Данные показали наличие и организацию везикул нейромедиаторов между пре- и постсинаптическими белковыми кластерами (рис. 2). Рисунок 2 (справа). Первичные корковые нейроны крысы культивировали в течение 14 дней, что позволяло формировать синапсы на чашке. Нейрональные синапсы были визуализированы в трехцветной визуализации методом dSTORM микроскопии с использованием двух пресинаптических белков Bassoon (пурпурный), VGluT1 (зеленый) и постсинаптический белок Homer1 (оранжевый). |
|
Часть 2
Моделирование болезни: визуализация одиночных молекул в тканях мозга
Сложность мозговой ткани при нейродегенерации
Наш мозг состоит из очень сложных и плотно упакованных тканей со специализированными функциями. Мозг взрослого человека содержит примерно 86 миллиардов нейронов и такое же количество поддерживающих клеток, включая астроциты и микроглию. В среднем каждая клетка мозга связана примерно с 25000 другими клетками, а это означает, что ткани объединены локальными переплетенными клетками, которые проецируются в отдаленные области. Это делает трехмерную (3D) визуализацию тканей мозга сложной задачей для нейробиологов.
|
Перед исследованиями тканей головного мозга стоит ряд проблем, которые обычно включают в себя отбор и подготовку образцов, маркировку образцов, визуализацию толстых срезов или сбор трехмерных данных, часто с использованием трудоемких протоколов. Текущие усилия также сосредоточены на использовании моделей стволовых клеток и молекулярных инструментов для имитации физиологии мозга и лучшего изучения происхождения неврологических расстройств. Текущие новаторские исследования сосредоточены на обнаружении и проверке биомаркеров ранних заболеваний в жидкостях человека, таких как спинномозговая жидкость, которые могут помочь диагностировать нейродегенеративные заболевания на ранних/предсимптоматических стадиях, учитывая высокую чувствительность обнаружения достигается базальный уровень биомаркеров (в большинстве случаев аттомолярные концентрации). Это также будет способствовать лучшему пониманию механизмов заболевания и позволит лучше стратифицировать пациентов перед терапией. В настоящее время проводятся ранние клинические испытания, чтобы проверить, как небольшие лекарства могут блокировать или стимулировать ключевые молекулярные взаимодействия, участвующие в прогрессировании нейродегенеративного заболевания. В последние годы внеклеточные везикулы также изучались как потенциальные переносчики молекул для межклеточной коммуникации внутри тканей и во всем теле, с их уникальной способностью преодолевать гематоэнцефалический барьер и облегчать связь между периферическими тканями и центральной нервной системой. |
Рисунок 3. Обзорное сканирование среза ткани мозга мыши. Изображение ткани мозга мыши толщиной 10 мкм. Ядра были помечены DAPI, а функция обзорного сканирования микроскопа Nanoimager использовалась для определения интересующей структуры - гиппокампа. Образец подготовлен Робертом Хиншоу, Центр неврологических заболеваний Энн Ромни, Бригам энд Женская больница, Бостон. |
Разрешение одиночных синапсов в ткани: матричная PALM томография
|
В средах с плотной тканью глубина часто влияет на рассеяние света. Высокое содержание липидов в мозге (более половины твердого вещества) способствует несоответствию показателя преломления, что вызывает рассеяние света. Очистка тканей - это подход к решению этой проблемы, однако он требует специальной подготовки и трудоемкой обработки, обычно выполняемой на срезах ткани толщиной >1 мм. Подходом к визуализации тканей, который позволяет проводить молекулярный и ультраструктурный анализ нейронных цепей в тканях, является матричная томография. Последние достижения в микроскопии сверхвысокого разрешения позволили разработать комбинированную томографию PALM как способ получения изображений глубоких тканей с высокой чувствительностью с помощью физического сечения и достижения изотропного высокого разрешения во всех трех измерениях. После идентификации уникальной структуры в качестве опорной точки в каждой из секций (Рисунок 4), положения могут быть отображены в более высокой детализации с помощью метода PALM для визуализации синаптических кластеров белков (т.е. кластеров PSD95) и определить их структуру и неоднородность в тканях мозга на одномолекулярном уровне (рисунок 5). Рисунок 4: Слева: Обзорное сканирование ультратонкого среза ткани головного мозга человека, помеченного mEOS-меченным PSD95, постсинаптическим белком. Это использовалось для определения уникальной структуры в каждой из секций (A-C), которая служила ориентиром для построения изображений
|
|
Маркировка одиночных молекул в тканях мозга
Мечение интересующих молекул in vivo может также стать серьезным узким местом для исследователей, особенно при подготовке образцов тканей для визуализации одиночных молекул. Для визуализации тканей мозга in vivo можно использовать различные подходы к маркировке, включая фотоактивируемые флуоресцентные белки (FP) или гало-теги. Гало-теги сочетают в себе преимущества генетически закодированных флуоресцентных белков с превосходной яркостью синтетических красителей и фотостабильностью.
Преимущество использования системы визуализации с одновременным получением двух цветов заключается в том, что можно напрямую сравнивать различные методы маркировки. В этом примере для оценки эффективности флуоресцентного мечения in vivo единичных молекул с использованием тегов Halo использовали PALM-визуализацию целых срезов ткани головного мозга мыши. Сравнение локализаций между фотоактивированным белком PSD95-mEos2 (синий) и меченой меткой PSD95-Halo (пурпурный) использовали для проверки эффективности метки Halo-tag in vivo.
/articles/Understanding the brain/Figure5-6802cc4ea3-2048x640.png)
Рисунок 6. Цельная ткань мозга мыши, помеченная двумя флуорофорами для оценки эффективности мечения in vivo. PALM-изображение среза мозговой ткани толщиной 6 мкм мыши PSD95-mEos2 / PSD95-Halo (синий и пурпурный, соответственно), меченного красителем HaloTag-PA Janelia Fluor® 646. Двухцветная визуализация PALM использовалась для оценки эффективности мечения постсинаптического белка с использованием тегов Halo in vivo (увеличенные области). Образец подготовлен Центром клинических исследований мозга Эдиты Буловайте (группа Сета Гранта), Эдинбургский университет, Великобритания.
Часть 3
|
Нейро-нановизуализация Микроскоп Nanoimager позволяет проводить нейровизуализацию одиночных молекул культивируемых нейрональных клеток и срезов тканей мозга с разрешением до 20 нм. Сочетание функций автоматизации с визуализацией сверхвысокого разрешения позволяет быстро и эффективно идентифицировать интересующую область для последующего сбора данных о локализации тысяч синаптических белков. Это также облегчает получение данных о распределении отдельных молекул, совместной локализации или профилях постсинаптической плотности. Поддерживая визуализацию как фиксированных, так и живых образцов, исследователи могут разработать свои собственные анализы для построения полного пространственно-временного портрета нейронных путей. Чувствительность к одной молекуле означает потенциал для улучшенной и ускоренной диагностики и лечения заболеваний. Понимание того, как лекарственные препараты изменяют механизмы и кинетику нейротрансмиссии при минимальных требованиях к образцам, также может привести к надежному, быстрому и эффективному составлению профилей лекарств более экономичным способом. Визуализация одиночных молекул может помочь установить и охарактеризовать новые модели заболеваний, чтобы сделать возможным надежное тестирование новых терапевтических средств и облегчить разработку лекарств. Благодаря своей компактной конструкции, отсутствию необходимости в темной комнате или дополнительной инфраструктуре, микроскоп Nanoimager является наиболее доступным инструментом сверхвысокого разрешения из когда-либо созданных. |
|
Выводы
Визуализация одиночных молекул открывает новые возможности в области нейровизуализации. Это дает исследователям новые инструменты для:
- Определения синаптической архитектуры в здоровых и пораженных болезнью тканях;
- Отслеживания динамики белков в живом мозге, одновременно визуализируя разные метки;
- Понимания молекулярных механизмов нейродегенерации тканей;
- Выявления основных маркеров, связанных с заболеванием, для улучшения ранней диагностики и определения новых целей для лекарств;
- Ускорение разработки лекарств и характеристики нейродегенеративных, психических или неврологических расстройств.

/articles/Understanding the brain/synapse@4x-dcdfdb6161.png)
/articles/Understanding the brain/single-molecule-neuroimaging-fa208a72dc-656x1024.png)
/articles/Understanding the brain/Figure3-ef8c238197.png)
/articles/Understanding the brain/Figure-4-1.png)
/articles/Understanding the brain/neuro-nanoimaging-7f0c27a3ef-600x1024.png)