Святой грааль световой микроскопии: улучшить разрешающую способность метода, чтобы можно было различать индивидуальные молекулы, находящиеся очень близко друг к другу. Микроскоп MINFLUX позволяет получать изображения, которые более чем в 100 раз четче по сравнению со снимками, полученными с помощью обычной световой микроскопии. Он превосходит даже лучшие на сегодняшний день методы световой микроскопии со сверхразрешением, а именно STED, разработанный Хеллом, и PALM/STORM, описанный нобелевским лауреатом Эриком Бетцигом, в 20 раз. В MINFLUX Хелл использовал преимущества STED и PALM/STORM в рамках совершенно новой концепции. Этот прорыв открывает перед исследователями новые возможности для изучения функционирования жизни на молекулярном уровне.
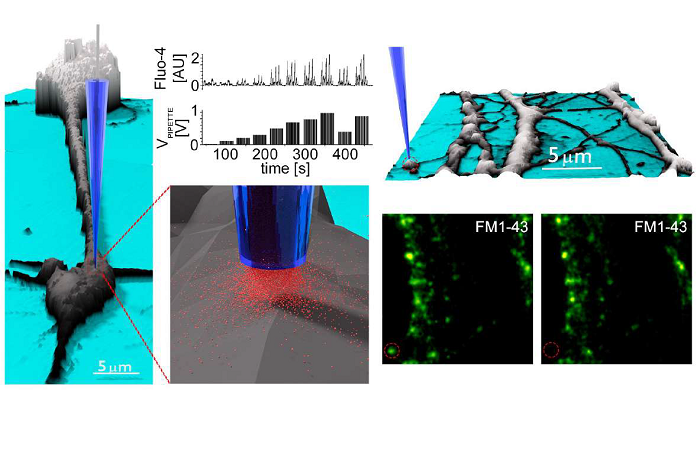
Метод, названный MINFLUX, основан на регистрации небольшого числа фотонов от единичной молекулы при ее возбуждении световым пучком в форме кольца («пончика») с центральной зоной субдифракционного размера (такое кольцо получают тем же способом, что и гасящий луч для STED/RESOLFT). Поскольку позиция кольца на поле зрения точно определена, для вычисления координат флуорофора достаточно всего нескольких фотонов, испущенных молекулой при ее возбуждении вблизи центра светового кольца при четырех положениях последнего (центр и вершины вписанного в кольцо треугольника). Получаемое разрешение зависит от диаметра светового кольца и числа детектированных фотонов (чем меньше диаметр и больше количество фотонов, тем лучше разрешение). Разрешающая способность MINFLUX намного превосходит таковую STED и SMLM. Так, при диаметре светового кольца 50 нм достаточно всего 30 и 500 фотонов для получения разрешения 5 и 1 нм, соответственно. MINFLUX характеризуется также чрезвычайно высоким временным разрешением (субмиллисекундная шкала). При этом молекулярный трекинг может производиться как в нанометровой шкале (внутри кольца), так и в микронной шкале путем перемещения центра кольца возбуждающего света вслед за движущейся молекулой. Это было продемонстрировано на примере слежения за подвижностью рибосом в живых бактериальных клетках. Следует подчеркнуть, что MINFLUX хорошо подходит для получения изображений только, малых полей зрения, сопоставимых по размеру с диаметром светового кольца.
"С помощью MINFLUX мы регулярно достигали разрешения в один нанометр, что составляет диаметр отдельных молекул - предел возможного во флуоресцентной микроскопии", - объясняет Хелл, директор MPI по биофизической химии. "Я убежден, что микроскопы MINFLUX имеют потенциал стать одним из самых фундаментальных инструментов клеточной биологии. С его помощью можно будет составлять карты клеток в мельчайших деталях и наблюдать за быстрыми процессами в их внутреннем пространстве в режиме реального времени. Это может произвести революцию в наших знаниях о молекулярных процессах, происходящих в живых клетках".
Геттингенский физик Штефан Хелл, который также работает в MPI для медицинских исследований и Немецком центре исследования рака в Гейдельберге, давно убедился, что разрешение флуоресцентной микроскопии может быть увеличено до размеров отдельных молекул - при классическом использовании сфокусированного света и обычных линз.

Слева направо: профессор Штефан Хелл, др. Франциско Бальзаротти, Иван Эйлерс, Клаус Гвош у микроскопа. © Irene Böttcher-Gajewski / Max Planck Institute for Biophysical Chemistry
Физик Эрнст Аббе в 1873 году сформулировал теорему о том, что разрешение световых микроскопов ограничено половиной длины волны света, что составляет около 200 нанометров. Более 100 лет спустя предел Аббе все еще остается актуальным, однако Хелл первым показал, что это ограничение может быть преодолено с помощью STED-микроскопии, которую он придумал в 1994 году и экспериментально подтвердил пять лет спустя.
STED, а также PALM/STORM, разработанные через несколько лет после этого, на практике достигают резкости разделения от 20 до 30 нанометров - примерно в десять раз лучше, чем предел Аббе. За разработку этих методов световой микроскопии сверхвысокого разрешения Хелл и Бетциг вместе с Уильямом Э. Мёрнером были удостоены Нобелевской премии по химии 2014 года.
Преимущества объединения STED, и PALM/STORM
И STED, и PALM/STORM позволяют разделить соседние флуоресцирующие молекулы, включая и выключая их одну за другой так, чтобы они излучали флуоресценцию последовательно. Однако эти методы различаются в одном существенном моменте: STED-микроскопия использует лазерный луч в форме пончика для выключения молекулярной флуоресценции в фиксированном месте образца, то есть везде в фокальной области, кроме центра пончика. Преимуществом является то, что луч пончика точно определяет, в какой точке пространства находится соответствующая светящаяся молекула. Недостатком является то, что на практике лазерный луч недостаточно силен, чтобы ограничить излучение одной молекулой в центре пончика. В случае PALM/STORM, с другой стороны, включение и выключение происходит в случайных местах и на уровне одной молекулы. Преимуществом здесь является то, что человек уже работает на уровне одной молекулы, но недостатком является то, что он не знает точного положения молекул в пространстве. Позиции приходится выяснять, собирая как можно больше фотонов флуоресценции на камеру; для достижения разрешения менее 10 нанометров необходимо более 50 000 детектированных фотонов. Поэтому на практике невозможно регулярно достигать молекулярного (один нанометр) разрешения.
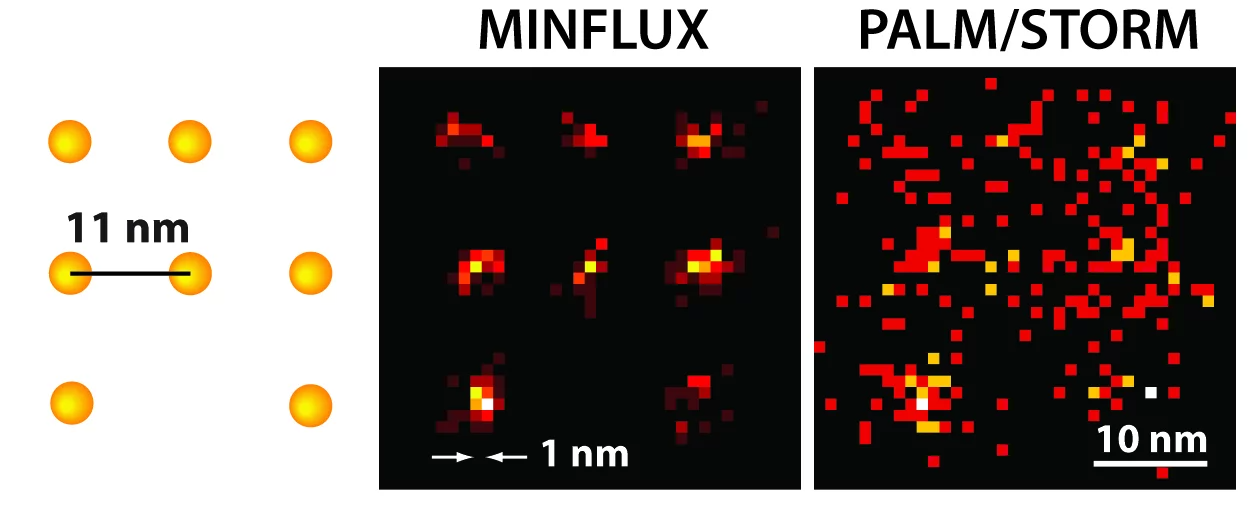
С помощью микроскопии MINFLUX впервые можно оптически разделить молекулы, находящиеся на расстоянии всего нескольких нанометров друг от друга. Здесь представлена схема флуоресцирующих молекул. В то время как микроскопия сверхвысокого разрешения PALM/STORM при той же яркости молекул (справа) дает диффузное изображение молекул (здесь в симуляции при идеальных технических условиях), положение отдельных молекул можно легко различить с помощью практически реализованной MINFLUX (в середине).
У Хелла возникла идея оригинальным образом объединить сильные стороны обоих методов в новой концепции. "Эта задача была далеко не тривиальной. Но мои коллеги Франциско Бальзаротти, Иван Эйлерс и Клаус Гвош проделали замечательную работу по экспериментальному воплощению этой идеи вместе со мной". Их новая методика, названная MINFLUX (MINimal emission FLUXes), теперь представлена Хеллом вместе с тремя младшими учеными в качестве первых авторов в журнале Science.
MINFLUX, как и PALM/STORM, включает и выключает отдельные молекулы случайным образом. Однако в то же время их точное положение определяется с помощью лазерного луча в форме пончика, как в STED. В отличие от STED, здесь луч в форме "пончика" (кольца) возбуждает флуоресценцию. Если молекула находится на кольце, она светится; если она находится точно в темном центре, она не светится, но ее точное положение определено. Бальзаротти разработал умный алгоритм, позволяющий определить это положение очень быстро и с высокой точностью. "С помощью этого алгоритма удалось использовать потенциал пучка возбуждения в форме "пончика" (кольца)", - объясняет молодой ученый. Гвош, который получил изображения с молекулярным разрешением, добавляет: "Это было невероятное чувство, поскольку мы впервые смогли различить детали с помощью MINFLUX в масштабе нескольких нанометров".
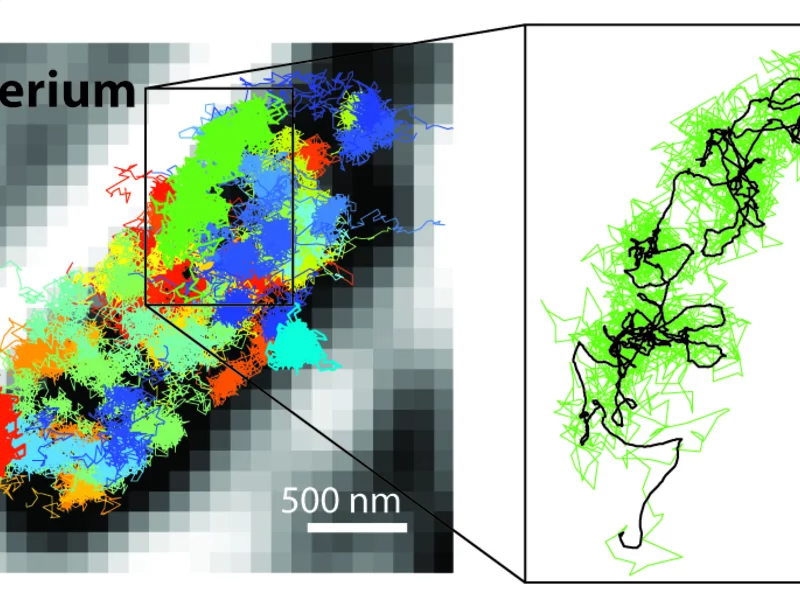
С помощью MINFLUX можно следить за многими гораздо более быстрыми движениями, чем это возможно при микроскопии STED или PALM/STORM. Таким образом, можно сделать движение меченных флуоресценцией молекул видимым в живой клетке. Слева: Схема движения 30S рибосом (цветные) в бактерии E. coli (черно-белое). Справа: Схема движения одной 30S рибосомы (зеленая), показанная в увеличенном виде.
В 100 раз лучшее разрешение
Помимо молекулярного разрешения, сочетание STED и PALM/STORM дает еще одно важное преимущество: "MINFLUX работает гораздо быстрее. Поскольку он работает с лазерным лучом в форме "пончика", ему требуется гораздо меньший световой сигнал, то есть меньше фотонов флуоресценции на молекулу, в сравнении с PALM/STORM для достижения максимального разрешения", - утверждает Хелл. С помощью STED уже можно было записывать видео в реальном времени изнутри живых клеток, но теперь стало возможным проследить движение молекул в клетке с временным разрешением в 100 раз лучше, как подчеркивает Эйлерс. Ему впервые удалось заснять движение молекул в живой бактерии E. coli с помощью MINFLUX с беспрецедентным пространственно-временным разрешением. "Что касается скорости, то мы не использовали все возможности MINFLUX", - говорит Эйлерс. Исследователи убеждены, что в будущем можно будет изучать даже чрезвычайно быстро происходящие изменения в живых клетках, например, движение клеточных наномашин или сворачивание белков.