Как добиться сверхразрешения
В конце концов, различия между PALM и STORM во многом исторические. Они были разработаны примерно в одно и то же время и получили два разных названия от своих изобретателей. На практике PALM и STORM часто используются как взаимозаменяемые понятия или объединяются под такими терминами, как "микроскопия мигания" или "микроскопия локализации одной молекулы" (SMLM). С точки зрения аппаратного обеспечения различия в любом случае нулевые. Оба метода требуют хорошей стойки микроскопа с сильным широкопольным освещением, высококлассного объектива и быстрой, чувствительной камеры.
Чтобы найти заметные различия между PALM и STORM, нужно сначала посмотреть, что у них общего: оба они являются типами флуоресцентных световых микроскопов сверхразрешения. Другими примерами таких микроскопов являются STED и MINFLUX, которые обладают еще большей производительностью.
В "обычном" флуоресцентном микроскопе разрешение ограничено примерно 200 нанометрами из-за дифракции. Дифракция размывает изображение отдельных молекул красителя, из-за чего молекулы, расположенные близко друг к другу, не видны по отдельности. Изображение становится нечетким, и детали за пределами дифракционного предела не могут быть обнаружены.
Все без исключения доступные методы сверхразрешения обходят эту проблему, манипулируя отдельными молекулами красителя таким образом, чтобы они не светились одновременно. Это, в свою очередь, делает возможным их раздельное изображение, несмотря на их размытость в результате дифракции. Существует примерно два подхода к этой манипуляции. На самом деле, их три.
Различные подходы
Исторически первым из них была STED-микроскопия, в которой второй "выключающий" пучок света в форме пончика обеспечивает темноту для всех излучателей - за исключением небольшого ансамбля в центре, в темном отверстии пончика, где нет выключающего света. В результате этого большинство молекул, которые в противном случае излучали бы одновременно, замолкают. Таким образом, повышается разрешение, причем преимущество этого метода в том, что он физически очень прямой и не требует математической обработки. STED является методом точечного сканирования и может модернизировать существующие лазерные сканирующие микроскопы.
Во-вторых, существуют методы, которые случайным образом удерживают флуоресцентные молекулы в темном состоянии большую часть времени. Затем они позволяют нескольким из них кратковременно загораться, так что в радиусе 200 нанометров только один эмиттер светится одновременно. Хотя его изображение остается размытым, его центр масс можно определить очень точно, а значит, и положение молекулы тоже ясно. PALM и STORM принадлежат к этой группе. Они делают множество снимков изолированных молекул на камеру и используют программные алгоритмы для определения их положения в автономном режиме. Все позиции, нанесенные на одно изображение, затем приводят к окончательной картинке высокого разрешения.
Прежде чем мы перейдем к третьему подходу, скажите, в чем теперь разница между PALM и STORM? Если коротко, то она невелика. Фактически, она заключается исключительно в типе флуоресцентной молекулы. В STORM используются органические красители (например, abberior FLUX, Alexa Fluor 647 или Cy5), которые стохастически мерцают при определенных химических условиях. Они присоединяются к целевой структуре, например, с помощью меченых антител и требуют специального буфера. Для PALM, с другой стороны, используются фотоактивируемые или -конвертируемые флуоресцентные белки (mCherry, mEOS и т.д.). Для этого клетку генетически модифицируют таким образом, чтобы при производстве собственных белков она сама присоединяла флуорофор. Это делает окрашивание живых клеток относительно простым. Для получения изображения случайное подмножество непересекающихся флуорофоров стохастически активируется и формируется изображение, после чего они обесцвечиваются, и формируется изображение следующего подмножества.
Краткий обзор
*с адаптивным освещением
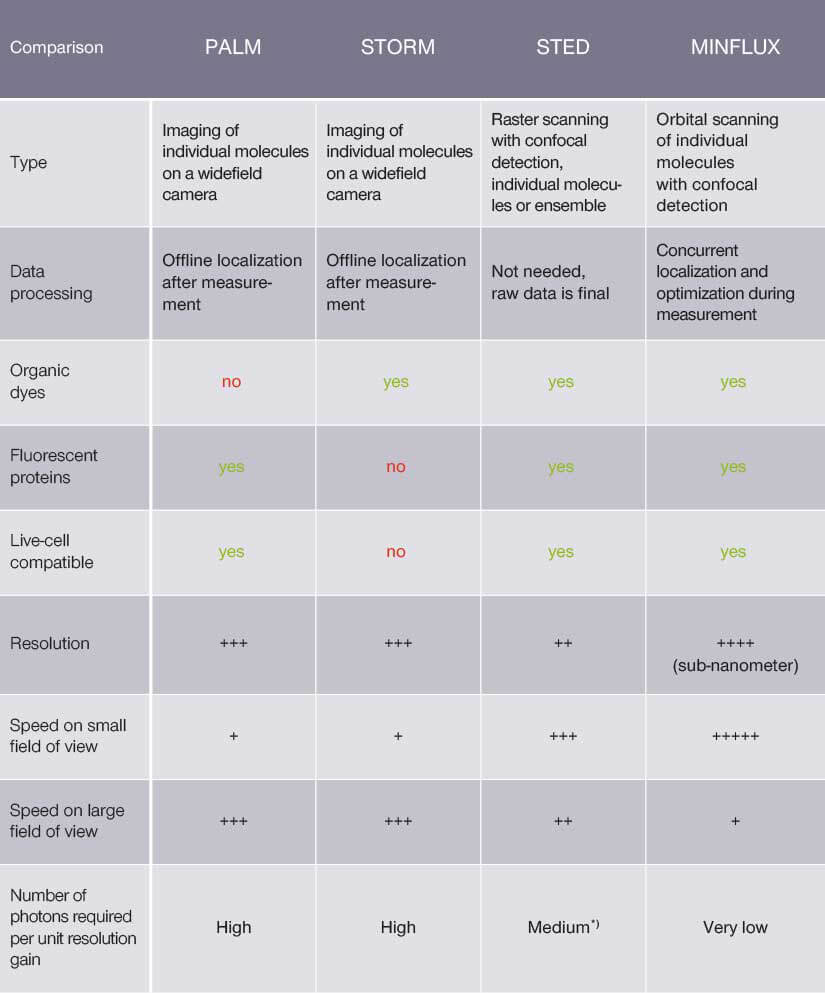
Сравнение PALM, STORM, STED и MINFLUX
При использовании обоих методов пользователь должен убедиться, что в ограниченной дифракцией области нет одновременно двух флуорофоров в излучающем состоянии; в противном случае они будут считаться как одна молекула в положении точно между ними. Для STORM это означает, что концентрация буфера должна быть отрегулирована так, чтобы молекул было достаточно, но не слишком много, чтобы избежать риска перекрытия. В случае PALM пользователь должен регулировать интенсивность активирующего лазера для достижения того же эффекта.
В целом, очевидно, что для того, чтобы вывести разрешение за пределы дифракционного предела, необходимо приложить определенные усилия. В PALM/STORM большая часть сложностей заключается в подготовке образца и правильном анализе необработанных изображений с камеры, за которые отвечает пользователь. В отличие от этого, STED требует более сложного оборудования, но ответственность за успех в большей степени лежит на стороне прибора. Хорошо, что коммерческие компании, такие как abberior, сегодня позаботились об этом, и использование приборов STED так же просто, как использование конфокального микроскопа.
Третий подход: MINFLUX
Но зачем нам сейчас нужен третий вариант? Он становится необходимым, когда PALM/STORM или STED достигают своих пределов. Хотя теоретически оба могут достичь беспредельного разрешения, на практике они этого не делают. Это происходит потому, что разрешение зависит от количества фотонов, а никакое количество фотонов не может стать произвольно большим. Их количество может быть большим, но оно не безгранично, как и разрешение. Но другая техника, MINFLUX, позволяет обойти эту проблему, сочетая преимущества мигающих молекул с преимуществами использования пучка света в форме пончика. MINFLUX гораздо более экономичен в использовании фотонов, чем PALM/STORM и STED, а сэкономленные средства можно вложить в более высокое, даже субнанометровое разрешение, и в гораздо более высокие скорости. Именно по этой причине MINFLUX имеет разрешение даже лучше, чем размер молекулы, и может измерять их положение несколько тысяч раз в секунду.