В настоящее время не существует надежного метода для захвата и подсчета всех ЦОК из-за их малого количества в крови (1-100 клеток/мл, что составляет не более 0,000002% всех клеток крови) и потому, что все существующие системы требуют первоначального выделения ЦОК или использования антител. Еще одним ограничением является их зависимость от экспрессии поверхностных маркеров EpCAMs (молекула адгезии эпителиальных клеток). Они экспрессируются на большинстве клеток первичных эпителиальных опухолей, но их экспрессия часто теряется во время прогрессии опухоли, то есть на стадии метастазирования.
Для решения проблемы микрофлюидное сообщество разработало новые технологии для работы с ЦОК, которые опираются на биофизические характеристики ЦОК. В частности, широко изучалось разделение на основе большего размера ЦОК по сравнению с другими клетками крови. Некоторые микрофлюидные чипы включают каналы сужения, массивы микрофильтров или массивы микрополостей типа "веер в веер" для захвата ЦОК. Однако эти чипы имеют ограничения по пропускной способности и эффективности захвата.

Рисунок 1: Микрофотография, изображающая морфологию клеточной линии рака простаты LNCaP-C4-2, экспрессирующей GFP.
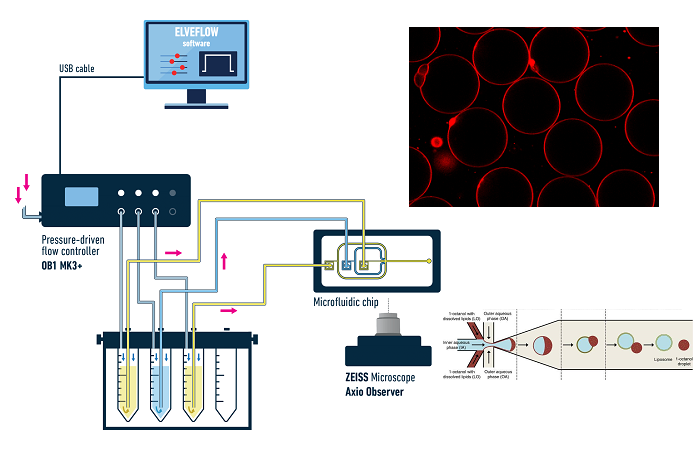
В свете предыдущих систем для ЦОК, Сян Рен и др. разработали новый чип для захвата ЦОК на основе разделения по размеру, который обеспечивает лучшую пропускную способность и эффективность захвата. Использование контроллера потока OB1 MK3 для захвата клеток рака простаты (LNCaP-C4-2) с эффективностью >95% при концентрации ~50 клеток/мл в крови мыши.
Применения
- Высокопроизводительное выделение циркулирующих опухолевых клеток;
- Точное определение количества циркулирующих опухолевых клеток;
- Ранняя диагностика рака простаты;
- Новые возможности создания чипов для других типов клеток (размеры каналов, количество каналов, подключение нескольких чипов...).
Материалы и методика
|
Высокопроизводительный чип для захвата ЦОК (CTC-HTECH)
|
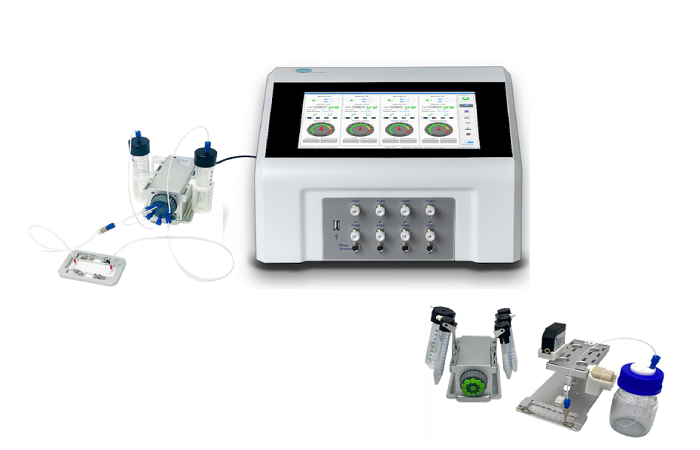
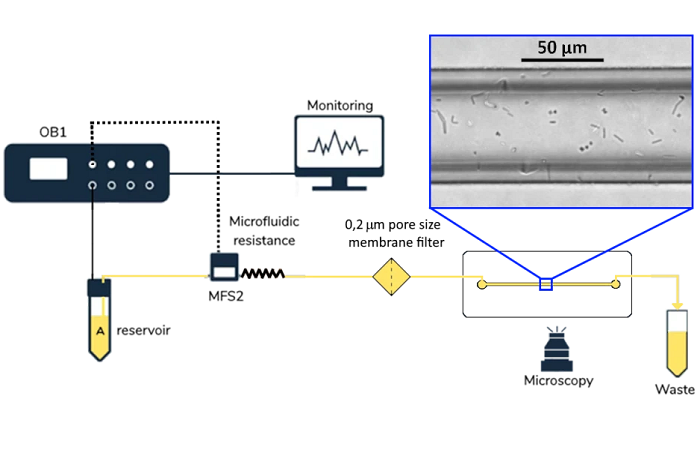
Установка

Методика
Чип CTC-HTECH состоит из одного блока полидиметилсилоксана (PDMS, полимер), полученного методом мягкой литографии и приклеенного к предметному стеклу с помощью плазменной обработки. Блок PDMS содержит сеть из 6 прямых параллельных каналов, соединенных серией из 40 сужающихся каналов. Каналы сужения, показанные в подразделе "Материалы", также показаны на рисунке ниже с примером 2 параллельных каналов (красный и синий).

Рисунок 2: Моделирование распределения давления вдоль чипа Circulating Tumor Cell-HTECH. (a) Распределение давления (Па) в ряду 1. Красный цвет соответствует высокому давлению, а синий - низкому. (b) Увеличенное распределение давления вблизи микроканалов (c) Увеличенное распределение давления в ряду 1 с клетками, захваченными в треппинг-камеры (выделены черными кругами) (d) Увеличенное распределение давления вблизи микроканала с клетками, захваченными в треппинг-камеры (каналы с клетками выделены черными кругами)
Каждый канал сужения состоит из 2 улавливающих камер (рис. 2d). Поскольку раковые клетки имеют схожий размер с улавливающими камерами, они деформируются в каналах сужения и восстанавливают свою форму в полостях улавливающих камер. Одиночные циркулирующие опухолевые клетки захватываются в этих улавливающих камерах, а остальные клетки проходят через микроканалы вместе с потоком крови. После прохождения всего образца крови камеры, содержащие ЦОК, сканируются (флуоресценция GFP), что позволяет определить общее количество ЦОК. Эта уникальная функция недоступна в других микрофлюидных чипах, основанных на размерах ЦОК.
С помощью контроллера OB1 MK3 Elveflow к резервуару с образцом крови было приложено постоянное давление 500 мбар. Результирующая скорость потока образца крови составляла ~ 2,4 мл/час. Изменяя подаваемое давление, насос OB1 поддерживает постоянное давление жидкости в системе. Это приводит к изменению скорости потока, поскольку клетки задерживаются в микроканалах, но позволяет избежать чрезмерного давления, которое создает дополнительное механическое напряжение и тем самым повреждает клетки (как это делают шприцевые насосы). Действительно, шприцевой насос создает режим постоянной скорости потока, гарантируя эффективность большинства микрофлюидных приборов с ограниченным числом микроканалов. Однако, увеличивая количество микроканалов в чипе CTC-HTECH, давление перераспределяется, вызывая механические силы сопротивления на захваченные клетки, изменяя прочность цитоскелета, жесткость мембраны и биомеханические свойства.
Результаты микрофлюидных исследований
На рисунке ниже показано устройство CTC-HTECH, состоящее из 6 рядов ①-⑥, упомянутых ранее, где ряд ① находится ближе всего к порту впуска крови. Выходы 1-6 были определены как места сбора отходов из рядов ①-⑥, соответственно. Во время каждого испытания открывался только один выход. Например, когда открывается выход 1, выходы 2-6 закрываются, циркулирующие опухолевые клетки задерживаются только в улавливающих камерах ряда ①, а выход 1 собирает другие клетки крови (рис. 3a). Когда открывается выход 2, ЦТК задерживаются в рядах ① и ②, а выход 2 собирает другие клетки крови.

Рисунок 3: (a) Иллюстрация конфигурации устройства (без масштаба) с входом, подключенным к контроллеру потока OB1 Mk3 компании Elveflow; каждый ряд и каждый выход были назначены и обозначены индивидуально. (b-g) GFP+ клетки рака простаты LNCaP-C4-2 (b) Изображение входного отверстия с GFP+ клеткой, начинающей входить в ряд 1 (c) GFP+ клетка в ловушке в ряду 1 после прекращения кровотока (d) Изображение сбора отходов на выходе 1 (e) GFP+ клетка деформируется и проходит через ряд 2 (f) Две GFP+ клетки в ряду 3, одна клетка все еще проходит, и одна клетка выходит из этого ряда (g) GFP+ клетка в ловушке в улавливающей камере ряда 4 (h) Общая эффективность захвата каждой розетки. Представленные здесь данные получены в результате 3 или 4 запусков на устройстве CTC-HTECH
Основной вывод из предыдущего рисунка заключается в том, что когда выход 1 был открыт и для захвата использовался только ряд 1, эффективность захвата составила 46,3% (рис. 3h зеленая полоса); когда выход 6 был открыт и для захвата использовались ряды 1-6, эффективность захвата составила 97,9% (рис. 3h красная полоса). Для достижения коэффициента улавливания >95% необходимо пять или шесть рядов микросужающихся каналов.
Авторы предположили, что с увеличением количества рядов общее сопротивление жидкости также увеличивается и, следовательно, эффективность захвата в каждом ряду варьируется. Так, когда использовался только выход 1, низкое сопротивление жидкости привело к увеличению скорости потока, который был слишком быстрым для захвата всех раковых клеток. Поэтому использование только пары рядов значительно снижает количество уловленных СТК.
Заключение
В этой публикации Сян Рен и др. представили новый чип для улавливания ЦОК на основе размера, повышающий эффективность улавливания. Эта недорогая система позволяет достичь эффективности захвата 96%. Это очень важно, так как было показано, что количество циркулирующих опухолевых клеток является диагностическим или прогностическим маркером опухоли. Время работы микрочипа составило ~30 мин для образца крови объемом 1,2 мл. По сравнению с магнитными частицами с антителами, такими как одобренная FDA система CellSearch, CTC-HTECH сокращает длительную предварительную обработку образца и время анализа ~4-6 часов.
Эффективность этого чипа гарантируется использованием контроллера потока OB1 MK3 Elveflow. Он может быть использован для обогащения и захвата CTC для клинической диагностики с помощью жидкой биопсии. Как настраиваемое устройство, этот чип может быть расширен в соответствии с тем же дизайном для повышения эффективности захвата, изменения размеров каналов, количества каналов, подключения нескольких чипов...