Динамическое культивирование клеток
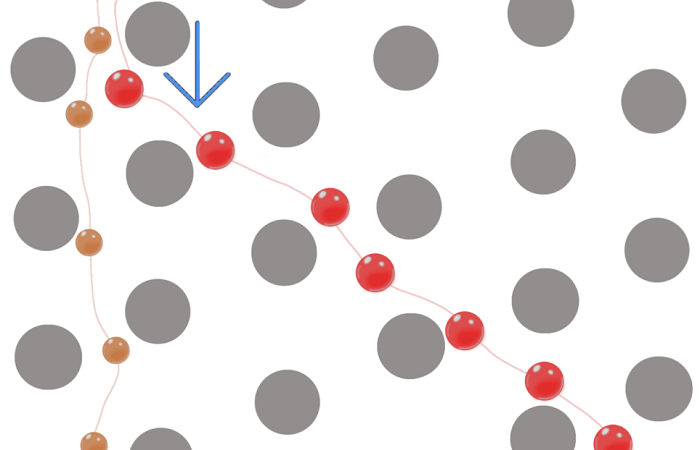
Такие силы, как растяжение, сжатие и напряжение сдвига, являются физиологически важными регуляторами клеточных реакций in vivo. Различия в диаметре и геометрии кровеносных сосудов по всему артериальному дереву объясняют широкий физиологический диапазон скоростей потока, профилей потока и напряжений сдвига в системе кровообращения. Интерстициальный поток через сети пористых тканей создает градиенты давления и напряжения сдвига. Поток жидкости по клеткам, культивируемым в микрофлюидных перфузионных камерах, обеспечивает ключевые механические стимулы, которые в значительной степени отсутствуют в традиционных методах культивирования. Важно отметить, что такие параметры, как скорость потока и напряжение сдвига, можно точно контролировать.
Преимущества микрофлюидной установки для клеточной биологии
Рециркуляция позволяет поддерживать более высокие скорости потока в течение нескольких дней, кондиционирование среды и исследования напряжения сдвига. Мы также рекомендуем к ознакомлению инструкции Elveflow по автоматическому введению клеток, микрофлюидной перфузии и окрашиванию клеток.
Примеры применений динамического потока для культуры клеток:
|
(например, кальциевый имиджинг, FISH);
- Скрининг на лекарственные препараты; - Напряжение сдвига; - Анализ адгезии клеток:
|
- Модели физиологии и заболеваний:
- И многое другое! |
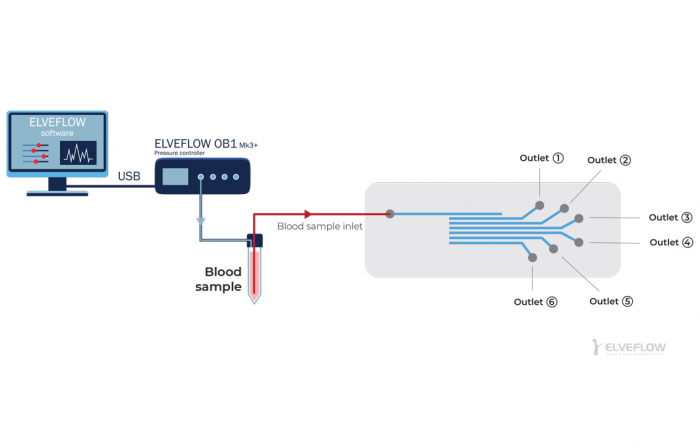
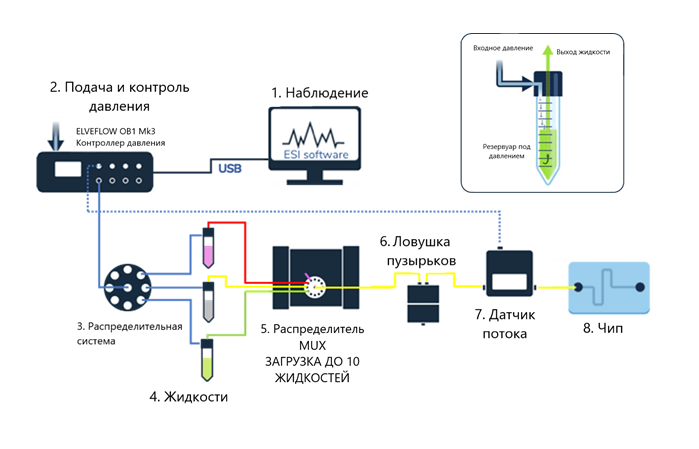
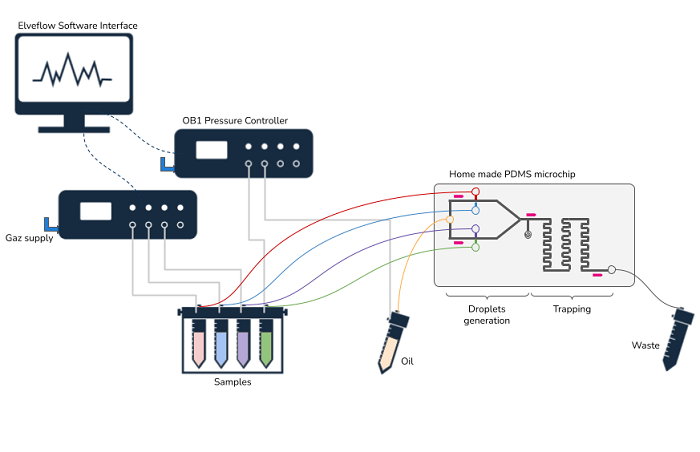
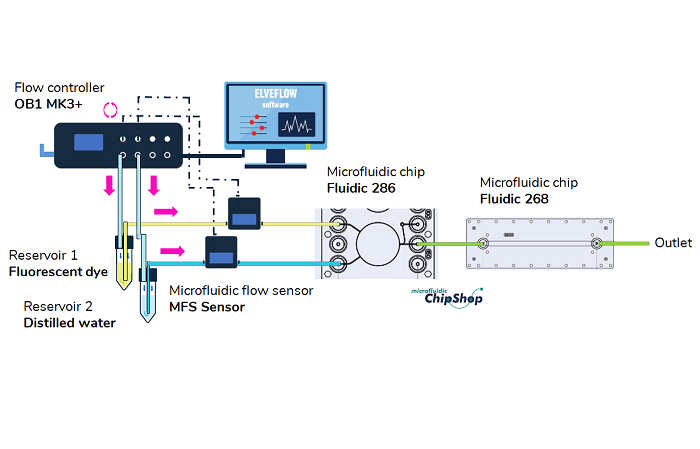
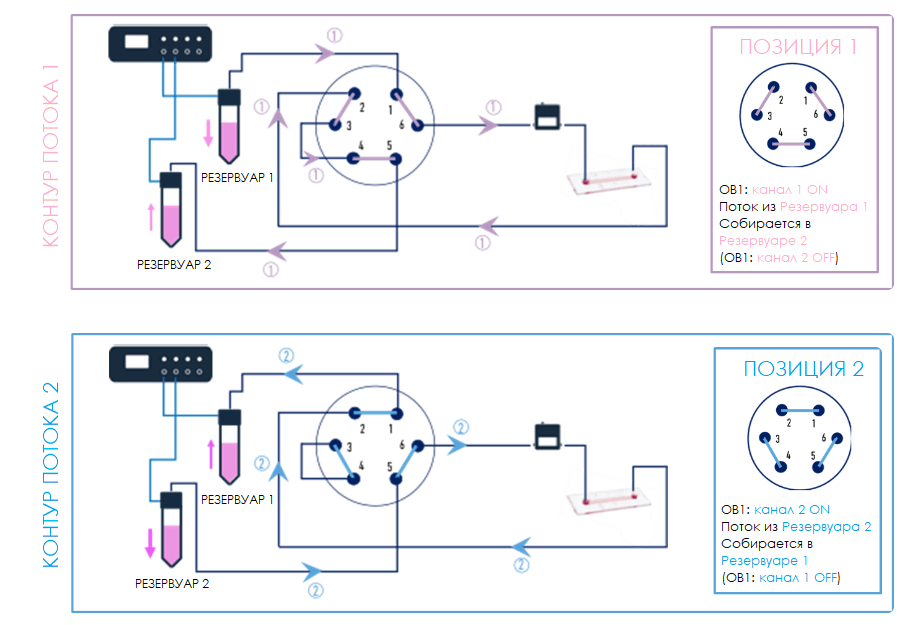
Схема установки рециркуляции среды
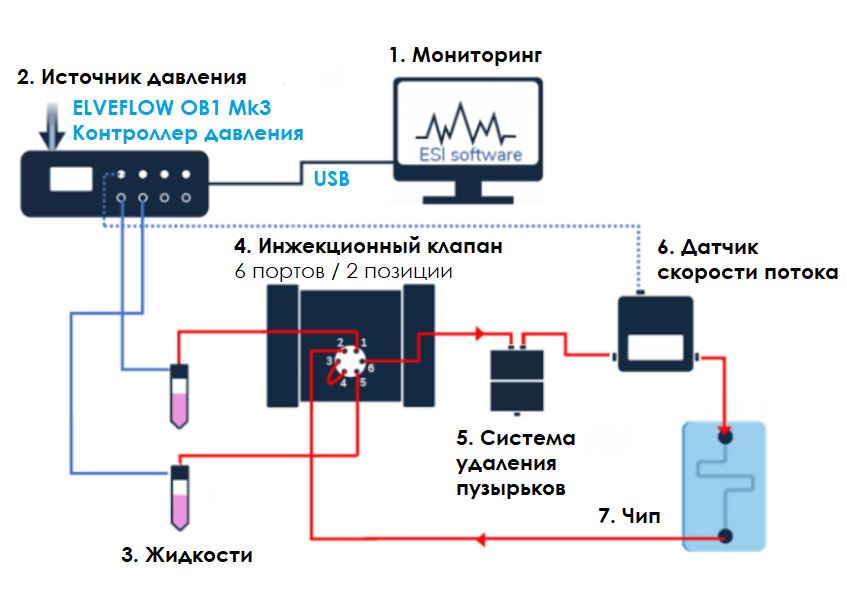
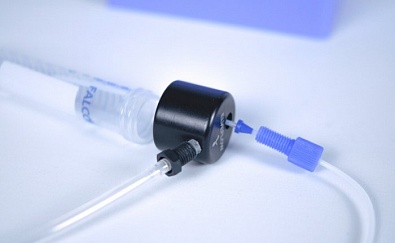
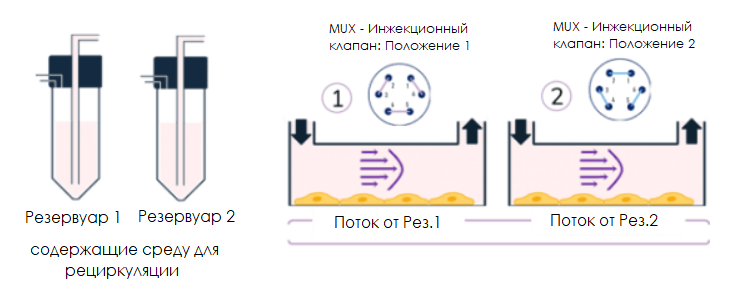
Инжекционный клапан MUX Elveflow: крупный план
Чередуйте позицию 1 и позицию 2 инжекционного клапана MUX. Жидкость течет из одного резервуара (под давлением) в другой (без давления). Поток через чип течет в одном направлении.
Список компонентов для установки рециркуляции
|
Реагенты:
|
Протокол рециркуляции среды
- Разместите клетки вручную с помощью пипетки внутри чипа. Оставьте их на 6-24 ч. для прикрепления.
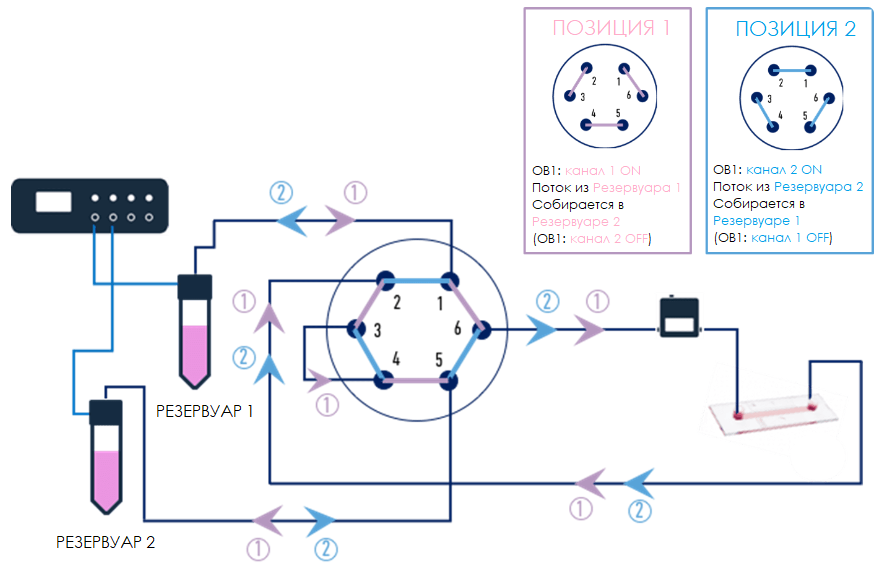
- Установите инжекционный клапан MUX Elveflow в положение 1.
- Поток: Начните выводить среду из резервуара 1 с помощью первого канала OB1 Elveflow. Резервуар 2 будет собирать поток из чипа. Перфузируйте в течение желаемого времени.
- Переключите инжекционный клапан MUX в положение 2.
- Поток: Начните поток от резервуара 2 с помощью второго канала OB1, сбросьте давление в резервуаре 1. Резервуар 1 будет собирать поток из чипа. Перфузируйте в течение желаемого времени.
- Повторите: Продолжайте циклически переключаться между положениями инжекционного клапана MUX, чтобы перфузировать клетки в течение желаемого общего времени.
Оба резервуара должны содержать среду в начале эксперимента: заполните резервуар 1 (исходный источник жидкости) примерно на 70% от общего объема и резервуар 2 (исходный коллектор жидкости) на 30%. Оставьте некоторый объем в резерве в резервуаре 1 перед переключением источников жидкости, чтобы избежать попадания воздуха в перфузионную камеру.
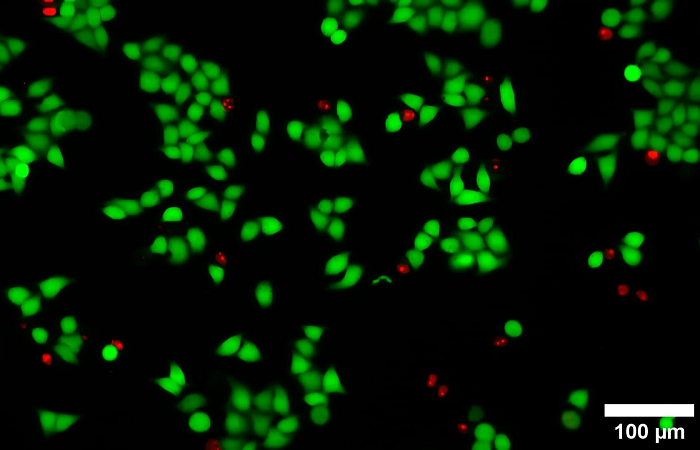
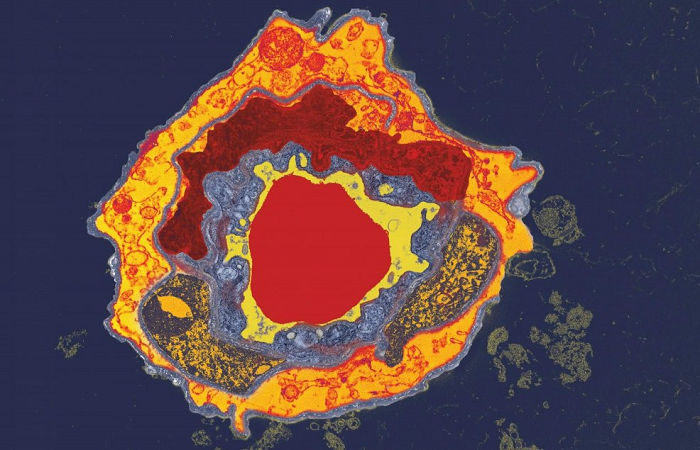
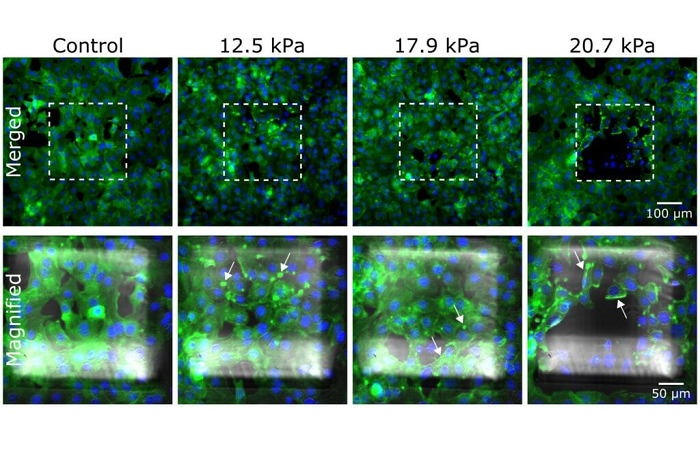
Результаты
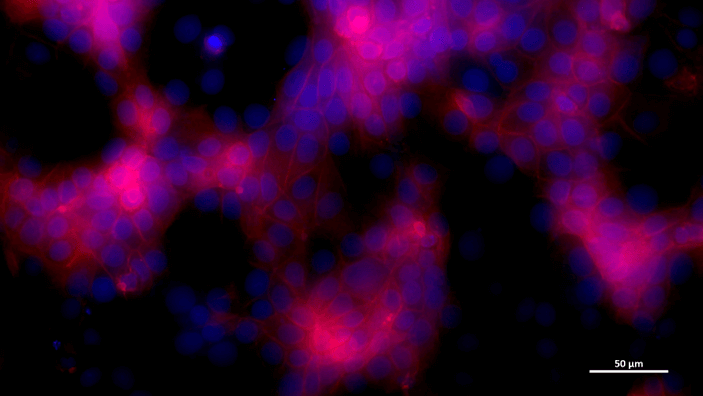
Клетки MCF7 выращивали при непрерывной рециркуляции среды (10 мкл/мин, 24 ч). Окрашены Hoechst/ родаминовым фаллоидином (зафиксированы PFA, 4%, пермеабилизирован BSA, 1%/ Triton X, 0,1%).
Наша команда экспертов может помочь вам провести эксперимент, улучшить конфигурацию установки для вашего конкретного применения и решить любые проблемы, с которыми вы можете столкнуться.
Мы можем вам помочь:
- Автоматизировать процесс с помощью планировщика в программе ESI;
- Использовать преимуществ напряжения сдвига;
- Удалить воздух и оставшиеся клетки;
- Контролировать перфузию с помощью давления или скорости потока;
- Увеличить продолжительность жизни клеток;
- Собрать схему для рециркуляции с использованием только микрофлюидных клапанов (без инжекционного клапана MUX);
- И многое другое!