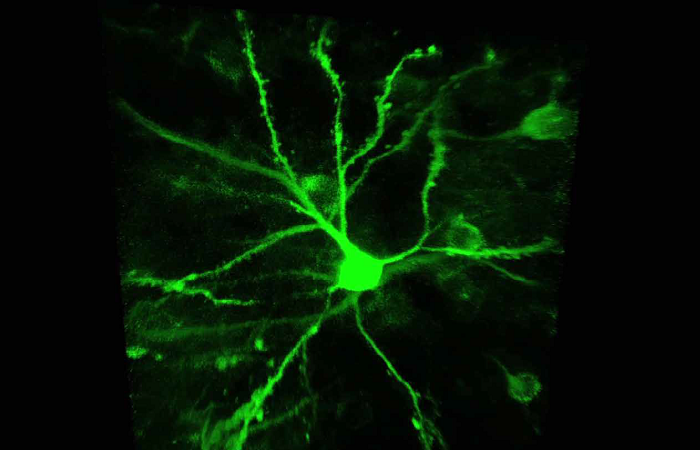
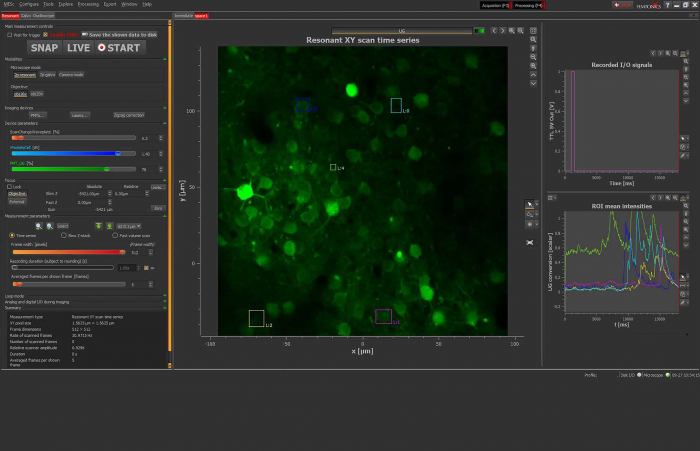
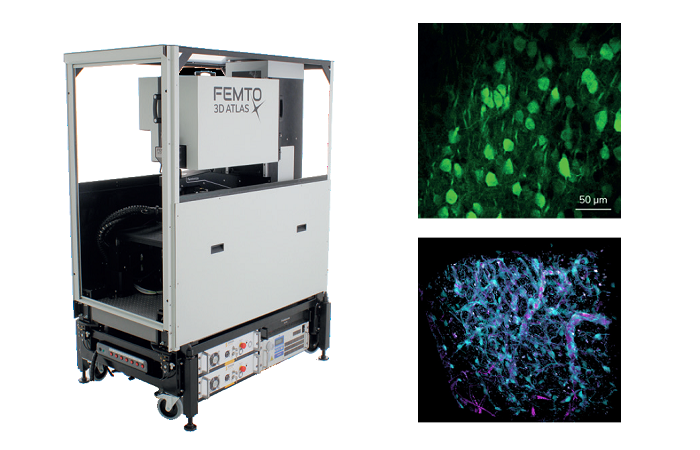
Флуоресцентная микроскопия широко используется в исследованиях, диагностике и биомедицинской визуализации. Она обеспечивает неинвазивную многомерную (X, Y, Z, t) визуализацию структур и молекул и идеально подходит для исследования медицинских и биологических образцов. К сожалению, разрешение обычных световых микроскопов ограничено дифракционным пределом (Abbe, 1873). Поэтому фундаментальным шагом стало появление методов сверхразрешающей флуоресцентной микроскопии, которые предлагают возможности разрешения за пределами дифракционного предела. В частности, STED - Stimulated Emission Depletion Microscopy (Hell and Wichmann, 1994) обычно разрешает структуры размером до 20 нм в самых разнообразных типах образцов, включая живые клетки, где визуализация клеточной динамики может дать важное понимание для биологии.
• Детектор MATRIX представляет собой массив плотно расположенных лавинных фотодиодов с высокой квантовой эффективностью.
• Он устраняет фоновую флуоресценцию и значительно повышает качество изображения и разделение объектов в плотных биологических структурах.
• Детектор MATRIX совместим со спектральным детектированием.
Сверхразрешающая микроскопия лучше всего подходит для областей, где сигнал вне фокуса минимален. Образцы с большей толщиной менее подходят для сверхразрешающей микроскопии из-за низкого отношения сигнала к фону. Детектор MATRIX Abberior Instruments устраняет это ограничение, подавляя фон вне фокуса, что позволяет получать 2D и 3D STED изображения с низким фоном даже для образцов с большой толщиной, плотным мечением и перекрывающимися структурами.
Задача: яркие изображения высокого разрешения с подавлением фона
Идеальный флуоресцентный микроскоп сочетает в себе множество функциональных возможностей и ключевых требований. Во-первых, микроскоп должен получать яркие флуоресцентные изображения. Для этого микроскоп должен быть оптимизирован таким образом, чтобы собрать как можно больше фотонов от флуорофоров в образце. Во-вторых, микроскоп должен получать сигналы только от одной плоскости. В 1950-х годах это привело Минского к изобретению конфокального микроскопа (Minsky, 1957). Однако на практике пинхол отклоняет не только свет из внефокусных плоскостей, но и часть света из фокальной плоскости (Egner et al., 2020). Важно отметить, что это не бинарное действие. Доля регистрируемого света уменьшается с расстоянием источника от фокальной плоскости, зависимость квадратичная. Поэтому для толстых образцов многие слои фона все еще могут суммироваться и вносить значительный вклад в нежелательный сигнал.
Третье требование - высокое разрешение. Было предложено несколько концепций для вычислительного улучшения пространственной информации конфокальных изображений (I. J. Cox and C. J. R. Sheppard, 1983), но эти стратегии в конечном счете ограничены доступными отношениями сигнал-шум (SNR) и отношением сигнал-фон в изображениях (SBR) (Sheppard et al., 1992). Теоретически улучшение разрешения также может быть достигнуто с помощью очень маленького отверстия пинхола (Schrader et al., 1996; Wilson, 1990). Однако это увеличение разрешения уравновешивается сильным уменьшением детектируемого света через пинхол, что снижает SNR и качество изображения. На практике эти методы имеют свои достоинства, но истинное преодоление дифракционного предела произошло только с появлением методов сверхразрешающей микроскопии, включая STED-микроскопию.
Увеличение разрешающей способности, обеспечиваемое STED-микроскопией, влечет за собой новые проблемы. В обычном микроскопе молекулы в пределах одного и того же фокусного объема испускают флуоресценцию одновременно и не могут быть разделены из-за малого разрешения. С увеличением разрешающей способности и, следовательно, уменьшением фокусного объема все меньше и меньше молекул испускают флуоресцентный сигнал одновременно. В конце концов, весь смысл сверхразрешения заключается в том, чтобы рассматривать небольшие структуры отдельно. Следовательно, уровень воспринимаемого сигнала будет падать, но только потому, что в каждый данный момент времени флуоресцирует меньше молекул. Тем не менее, STED действует только на флуорофоры в фокальной плоскости, в то время как флуорофоры в других слоях не деактивируются. Это приводит к тому, что сигнал регистрируется из фокальной плоскости с улучшенным разрешением, но уменьшенной интенсивностью, в то время как фоновый сигнал, исходящий от всей толщины образца, вносит свой вклад с полной интенсивностью.
Решение: MATRIX STED
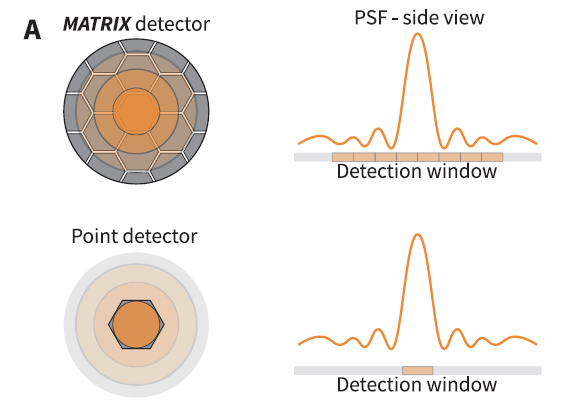
Детектор MATRIX Abberior Instruments является ключевым компонентом MATRIX STED, современного 3D-микроскопа STED с превосходным подавлением фона. Он состоит из нескольких лавинных фотодиодов (ЛФД), каждый из которых обладает необычайно высокой квантовой эффективностью (>50% при 500 нм), расположенных гексагонально на одном детекторном чипе (рис. 1). В отличие от обычной конфокальной и STED-микроскопии, MATRIX визуализация выполняется с открытым отверстием, так что собирается максимальное количество света от образца. Каждый из элементов записывает часть функции точечного разброса (PSF) – примерно 0.3 AU на отдельный элемент MATRIX.
 |
|
Рисунок 1. Принцип работы MATRIX.
(А) Матричный детектор состоит из более чем 20 отдельных элементов, которые позволяют обнаруживать сигнал в фокальной плоскости вместе с сигналом из плоскостей выше или ниже. Множество отдельных элементов создают большую детекторную матрицу, которая регистрирует центр PSF, а также его боковые части. По сравнению с точечным детектором регистрируется гораздо больше информации о PSF. (B) Принцип работы детектора MATRIX Abberior Instruments заключается в обнаружении и подавлении фона вне фокуса. В отличие от отверстия пинхола, которое может ограничивать только рассеянный свет от относительно удаленных друг от друга структур, MATRIX позволяет удалять рассеянный свет от соседних структур в плотных областях образца.
Обработка изображений может быть дополнена алгоритмом постобработки для лучшего качества и четкости изображения. Например:
1. Дифференциальное обнаружение: Данные, полученные с помощью детектора MATRIX Abberior Instruments, могут быть эффективно использованы для отличия сигналов из фокуса и вне фокуса. С помощью этой информации фон вне фокуса может быть удален из полученных изображений.
2. Деконволюция: В отличие от изображений конфокальных микроскопов с точечными детекторами, изображения, полученные с помощью детектора MATRIX Abberior Instruments, содержат большое количество дополнительной информации. В частности, известно количество сигнала от фокальной плоскости по сравнению с внефокусными вкладами. Эта дополнительная информация приводит к значительно улучшенным результатам при применении дальнейших этапов постобработки, таких как деконволюция.
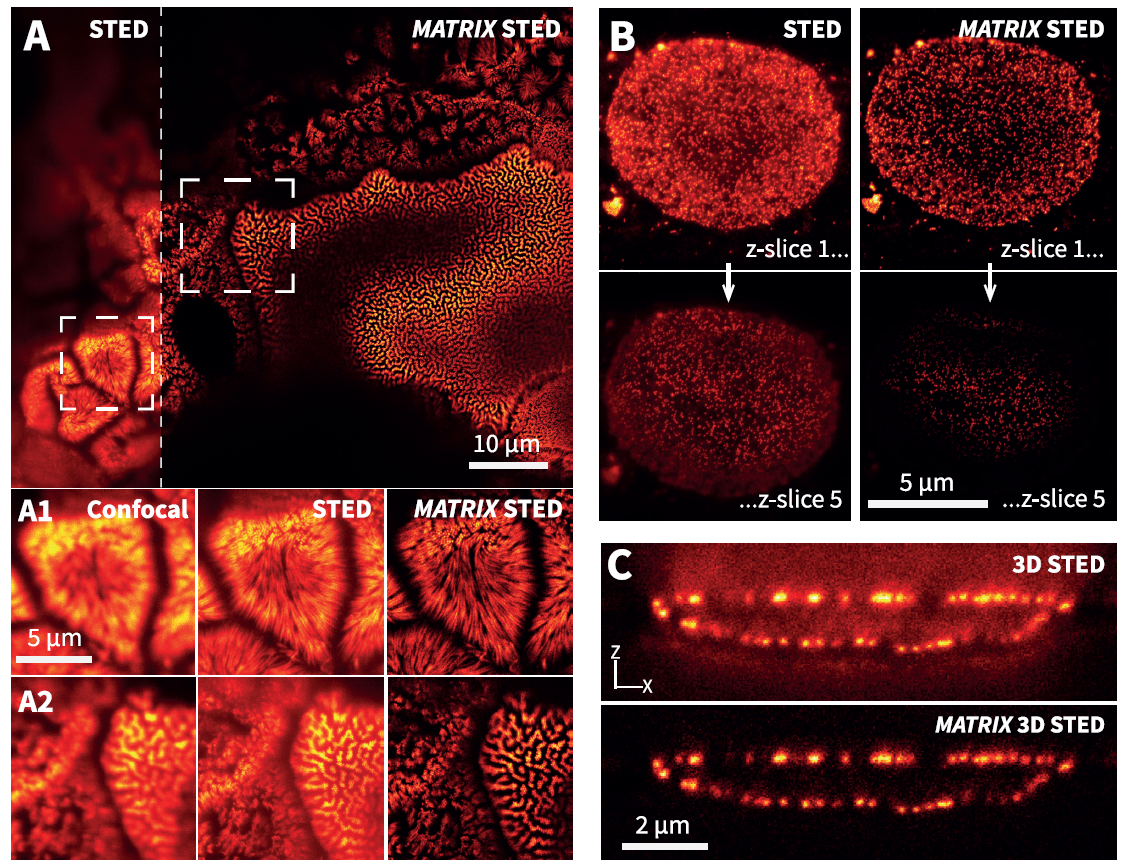
Рисунок 2. MATRIX STED улучшает четкость и качество STED.
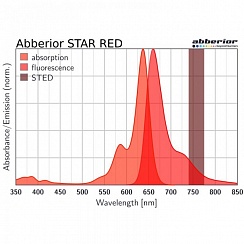
(А) Улучшенная четкость сигнала в 3D-модели культуры кишечных эпителиальных клеток. Сравнение конфокального, STED и MATRIX STED (A1-A2) показывает улучшенное отношение сигнала к фону за счет постобработки MATRIX. Клетки Caco-2, меченные фаллоидином-abberior STAR RED. (B) Оптический слайсинг хорошо получается при STED. А постобработка MATRIX позволяет удалять структуры, которые не находятся в фокальной плоскости. Показаны STED-стеки ядерных поровых комплексов в клетках млекопитающих (C) Улучшенное z-сечение является ключевым преимуществом 3D-объемной визуализации STED, поскольку уменьшение размытия вне фокуса позволяет улучшить 3D-разделение и 3D-рендеринг с повышенной четкостью сигнала. 3D STED z-сканирование белков ядерного порового комплекса в клетках млекопитающих. Изображения были получены с сопоставимым размером пинхола около 0,7 AU. Иммуномечение проводили с помощью abberior STAR RED.
Начиная с более четкого и лучшего изображения по сравнению с микроскопами с обычными точечными детекторами, микроскопы, оснащенные детекторами MATRIX Abberior Instruments, предлагают пользователям преимущество анализа изображений, включая улучшенное разделение плотно расположенных объектов, улучшенный подсчет частиц, оценку размера, измерение интенсивности, сглаживание и деконволюцию. Хотя удаление фона теоретически может быть достигнуто только одной деконволюцией, на практике трудно выполнить два требования: во-первых, алгоритмы деконволюции требуют очень точных знаний о форме функции точечного разброса (PSF) вдали от фокуса. Крошечные отклонения, вызванные аберрациями или неоднородностями образца, могут иметь большие последствия, которые могут привести к неточным результатам. Во-вторых, деконволюция требует записи 3D-стеков по всей толщине образца или, по крайней мере, по всей толщине, от которой происходит вклад фонового сигнала. Это значительно замедляет поглощение и увеличивает обесцвечивание и фототоксичность. С помощью MATRIX STED вклады фонового сигнала могут быть непосредственно считаны и удалены из xy-плоскости, без полного знания о фактическом PSF.
MATRIX STED в биомедицинских приложениях
В биологии области интереса часто представляют собой плотно упакованные зоны внутри клеток и тканей, так как именно эти зоны с наиболее плотным скоплением органелл или белков являются местами высокой биологической активности. В областях с низкой плотностью, таких как внешняя часть клетки, где органеллы и нити часто не перекрываются, сверхразрешающая микроскопия превосходна и позволяет очень хорошо разрешать и различать структуры. Однако области с высокой плотностью меченых структур трудны для исследования, поскольку вклад флуоресценции от соседних структур (в 3D) затрудняет однозначное разделение отдельных структур (рис. 2).
Уменьшение фона, предлагаемое MATRIX STED, выгодно для таких применений и типов образцов, где переполненные мембраны и органеллы могут генерировать фоновую дымку при изображении с помощью обычной микроскопии STED.
Например, мы показываем на рис. 2А обычную и MATRIX STED - визуализацию эпителиальных клеток Caco-2, меченных актином. Эти поляризованные клетки выращиваются на бумажной матрице и характеризуются множеством плотно упакованных клеточных выступов, называемых микроворсинками. С помощью MATRIX STED можно значительно улучшить отделение микроворсинок от фона (рис. 2 А1-А2), что позволяет улучшить 3D-визуализацию по сравнению с обычным STED. Кроме того, при визуализации белков в ядерной мембране, как показано на рис. 2B для белков ядерного порового комплекса MATRIX STED удаляет флуоресцентные вклады из ядерных пор, которые не находятся в фокальной плоскости, тем самым повышая z-секционирующую способность 2D STED далеко за пределы того, что возможно с помощью пинхола. Эффект удаления фона и усиленного разделения в z также очевиден с помощью 3D STED (рис. 2С). В целом, удаление внефокусного света с помощью MATRIX детектирования уменьшает распространение внефокусных структур в каждой отдельной z-плоскости и улучшает разделение плотно упакованных и меченых объектов, таких как элементы цитоскелета или митохондрий вблизи ядра.
Другим применением MATRIX STED является разделение белковых комплексов в синапсах, показанных на рис. 3А, где синаптический белковый Bassoon визуализируется вместе с актином для визуализации синаптических бутонов. Маркировка спектрином дополнительно подчеркивает цитоскелет нейрональных процессов. Селективное удаление фона с помощью MATRIX детектора улучшает разделение этих структур, а также обеспечивает значительно более высокие уровни сигнала в фокусе по сравнению с точечным детекторным изображением. Кроме того, для маркировки нескольких элементов цитоскелета, таких как виментин и актин, повышенная четкость и разделение нитей позволяет улучшить анализ и количественную оценку, особенно в областях, где многие нити перекрываются (рис. 3Б). В общем, это возможно для всех структур с высоким фоном, таких как кусочки ткани или плотно упакованные клеточные агрегаты.
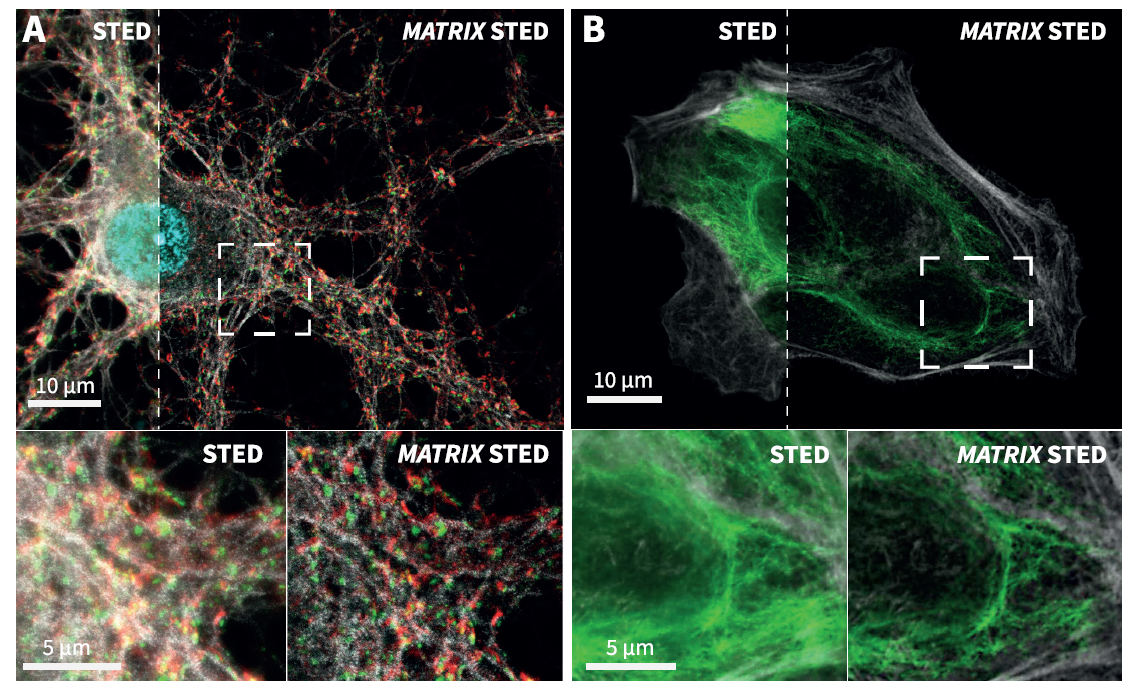
Рис. 3. Примеры MATRIX STED из нейробиологии и клеточной биологии.
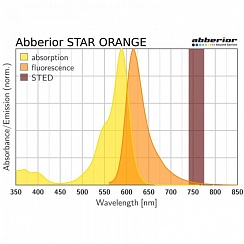
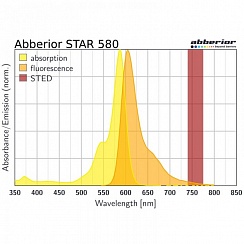
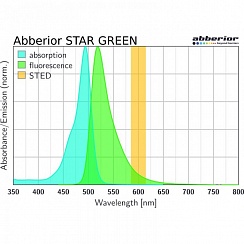
(А) Первичные нейроны, меченые спектрином (серый), Bassoon (зеленый), Dapi (голубой) и актином (фаллоидин, красный). (В) MATRIX STED Виментина (зеленый) и актина (фаллоидин, серый) в клетках млекопитающих демонстрирует преимущества детектирования для визуализации плотно упакованных структур, таких как элементы цитоскелета, например, виментин или фаллоидин. Улучшено разделение отдельных нитей, z-секционирование. Мечение: Нейроны (А): Первичное антитело против Bassoon и Спектрина, меченное вторичными антителами с abberior STAR RED и abberior STAR ORANGE, Фаллоидин был непосредственно связан с abberior STAR GREEN. (Б): Клетки млекопитающих с Виментином и Фаллоидином, меченные вторичными антителами с abberior STAR RED и abberior STAR 580.
Мысленный эксперимент
Этот простой эксперимент иллюстрирует преимущество матрицы детекторов, по сравнению с одним детектором: (1) Вытяните руку перед собой и вытяните большой палец руки, как на рисунке слева. (2) Сосредоточьтесь на большом пальце одним глазом (в то время как другой глаз закрыт). (3) Смотрите попеременно то одним, то другим глазом. Когда меняете глаз, ваш большой палец меняет положение относительно фона. Это показывает, что наличие двух глаз (двух детекторов) позволяет легко отличить передний план от заднего. Точно так же более двадцати “глаз” (детекторов) MATRIX могут быть использованы для определения фона для каждого пикселя и его подавления.

Заключение
Матричный детектор удаляет фон и увеличивает оптическое секционирование. Сочетание одного или двух MATRIX детекторов со спектральным RAINBOW детектированием дает превосходное качество изображения STED для плотно упакованных образцов и позволяет пользователю исследовать большое разнообразие красителей и экспериментальных условий, включая визуализацию фиксированных клеток, живых клеток и тканей.